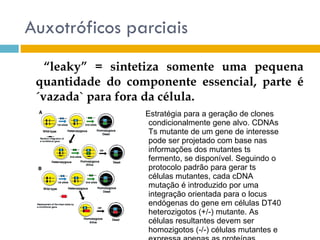
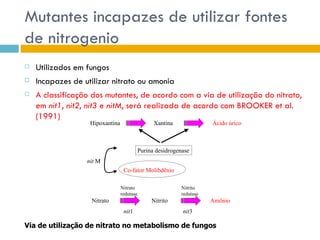
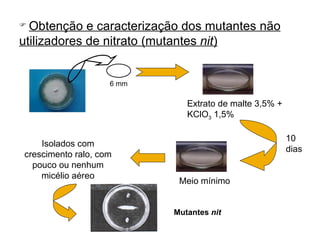
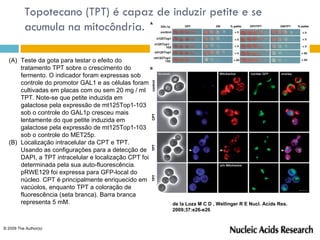
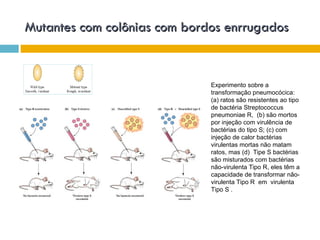
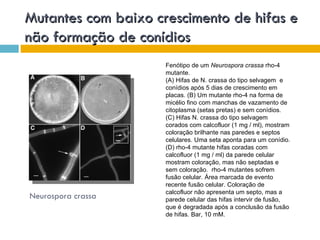
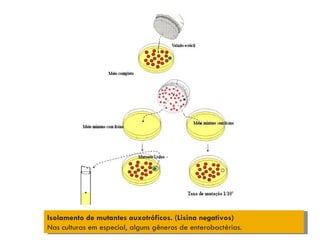
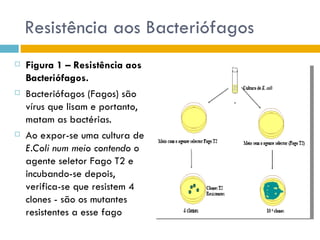
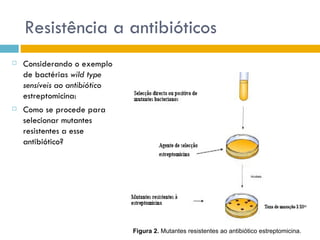
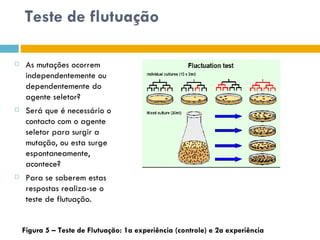
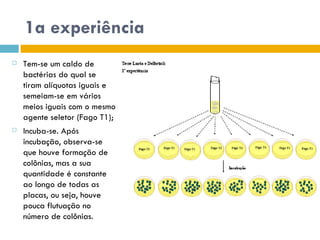
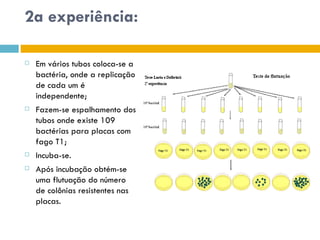
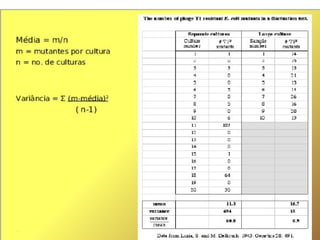
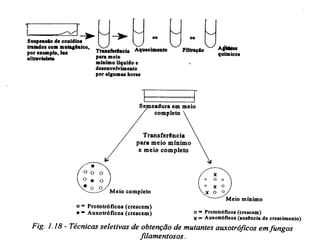
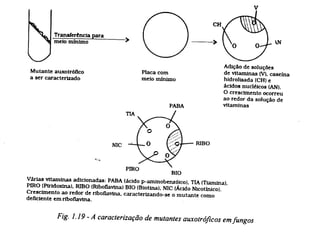
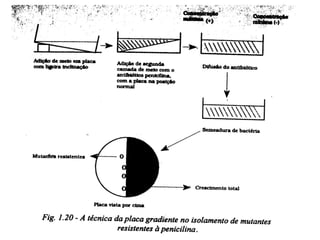
O documento discute como as mutações em microrganismos geram variabilidade e contribuem para a evolução. As principais formas de variação genética incluem mutações, recombinações e aquisição de novos genes. Os mutantes auxotróficos, resistentes a antibióticos e com alterações morfológicas são úteis para estudos genéticos de microrganismos.