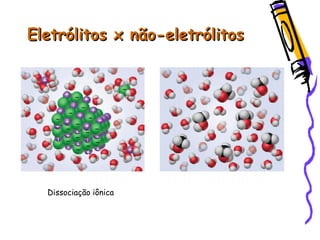
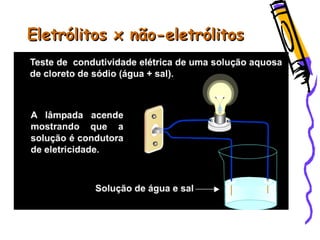
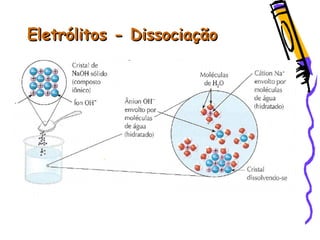
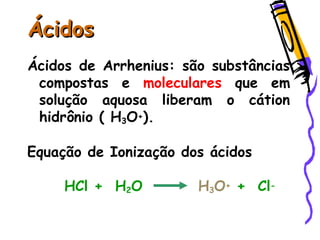
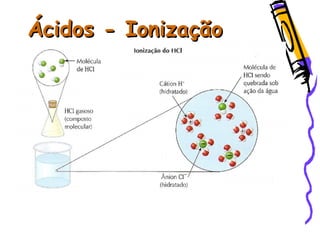
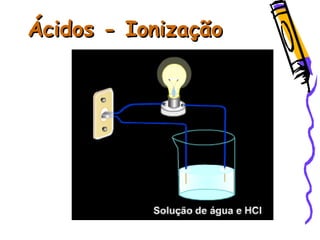
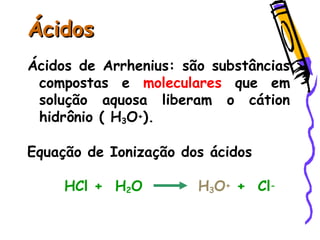
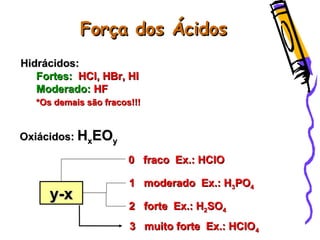
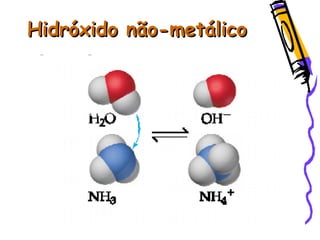
O documento resume as principais funções inorgânicas como ácidos, bases, sais e óxidos. Detalha as propriedades dos ácidos e bases segundo as teorias de Arrhenius, exemplificando alguns ácidos e bases importantes como o ácido sulfúrico, clorídrico, fosfórico, sódio e cálcio.