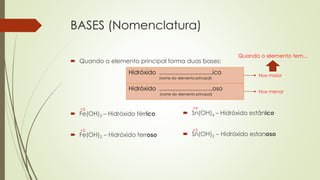
Este documento resume a nomenclatura de ácidos e bases inorgânicas. Explica que ácidos liberam íons hidrogênio em solução aquosa e bases liberam íons hidróxido. Fornece as regras gerais para a formulação de ácidos e bases e detalha a nomenclatura de hidrácidos, oxiácidos e hidróxidos com base no elemento químico e seu estado de oxidação. Por fim, apresenta exercícios para aplicar as regras de nomenclatura aprendidas.