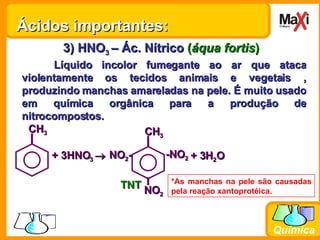
O documento descreve as principais funções inorgânicas, focando nos ácidos. Discorre sobre a definição de ácido, sua classificação, nomenclatura e exemplos importantes como o ácido sulfúrico, clorídrico, nítrico e fosfórico. Explica como os ácidos ionizam e liberam íons hidrogênio em solução aquosa.





![Classificação dos Ácidos Quanto ao número de elementos Químicos: Binário (HCl, HBr, HF) Ternário (H 2 SO 4 , H 3 PO 4 , HCN) Quaternário (H 4 [Fe(CN) 6 ]) Quanto ao número de Hidrogênios Ionizáveis: Monoácidos (HCl, HI, H 3 PO 2 ) Diácidos (H 2 SO 4 , H 2 S, H 3 PO 3 ) Triácidos (H 3 PO 4 , H 3 BO 3 , H 3 BO 2 ) Tetrácidos (H 4 P 2 O 7 )](https://image.slidesharecdn.com/resumo-cidos-4224/85/Resumo-Acidos-6-320.jpg)