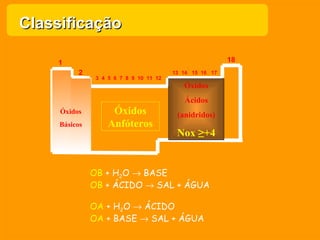
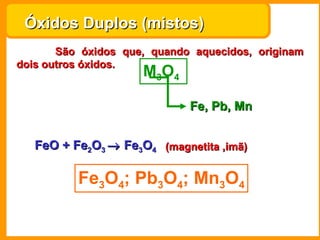
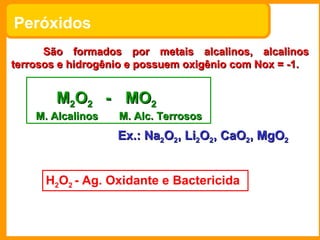
1) O documento descreve as principais funções inorgânicas - ácidos, bases, sais e óxidos, definindo suas propriedades químicas e classificações.
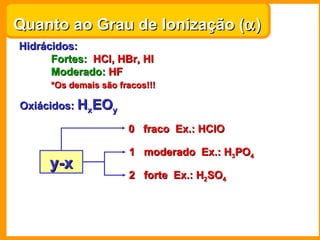
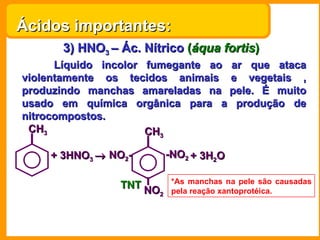
2) Ácidos são substâncias que liberam íons hidrogênio em solução aquosa. Exemplos importantes são os ácidos sulfúrico, clorídrico, nítrico e fosfórico.
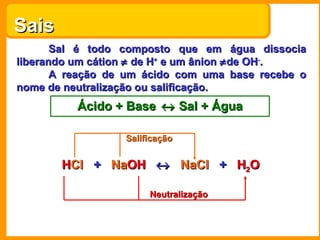
3) Bases são substâncias que liberam íons hidroxila em solução aquosa. Exemplos importantes são os hidróxidos de sódio, c