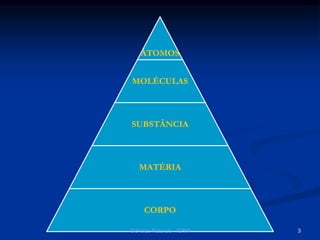
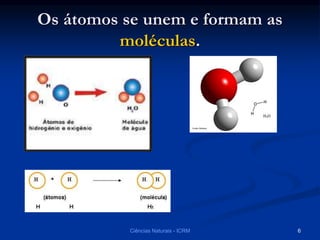
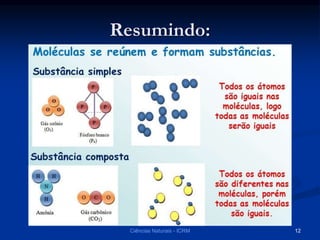
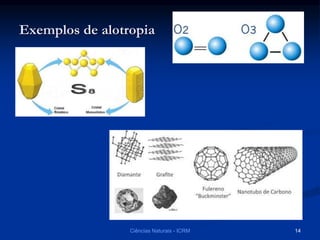
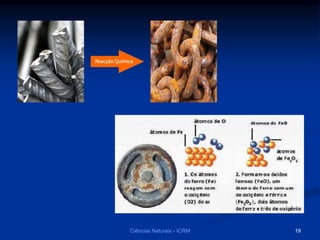
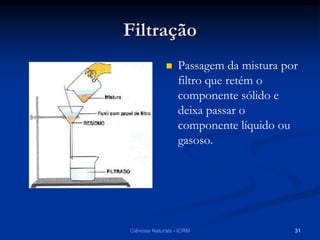
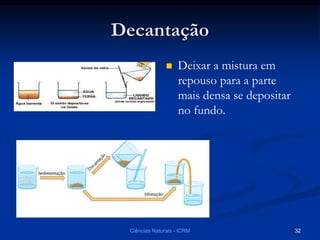
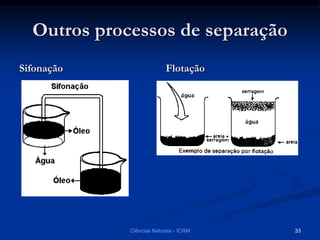
O documento explora a classificação das substâncias naturais, diferenciando entre substâncias puras, simples e compostas, além de discutir o fenômeno da alotropia. Também são abordados os conceitos de combinações e misturas, explicando como elas podem resultar em novos compostos ou manter as propriedades das substâncias originais. Métodos de separação de misturas, como filtração, decantação e destilação, são apresentados como processos para obter compostos ou componentes puros.