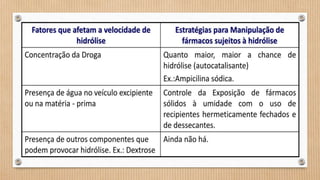
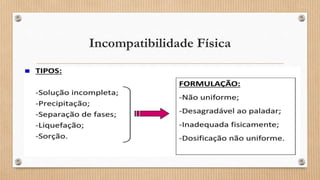
O documento discute tipos de incompatibilidades farmacêuticas, incluindo: (1) Incompatibilidade química, que ocorre quando substâncias formam novos compostos alterando propriedades; (2) Incompatibilidade física, quando uma mistura é não-homogênea devido à insolubilidade; (3) Incompatibilidade terapêutica, quando associações medicamentosas prejudicam o tratamento.


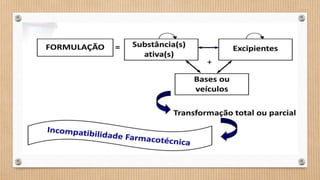





![Incompatibilidade Química - Oxidação
Reações de Oxidação
• Em química orgânica (portanto, para a maioria dos fármacos), oxidação é
frequentemente considerada sinônimo de perda de hidrogênio da molécula
(dehidrogenação).
• O processo oxidativo frequentemente envolve radicais livres, moléculas ou átomos
contendo um ou mais elétrons desemparelhados, assim como o oxigênio molecular
[O-2 (O-O-) e hidroxila livre (OH-)]. O processo oxidativo se dá em cascata (reação
em cadeia).](https://image.slidesharecdn.com/incompatibilidades-210507113500/85/Incompatibilidades-9-320.jpg)