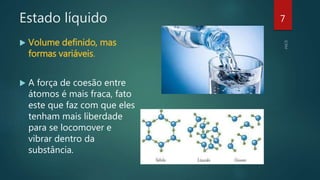
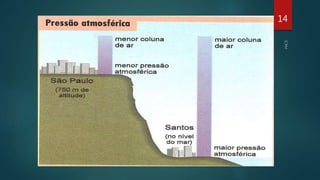
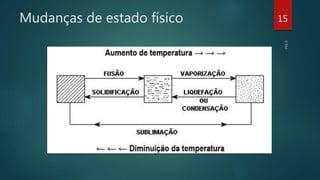
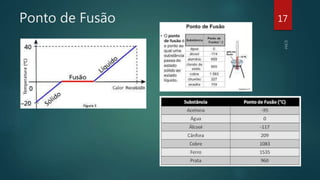
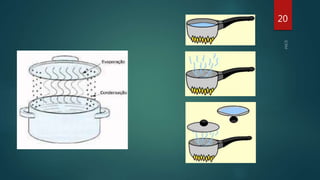
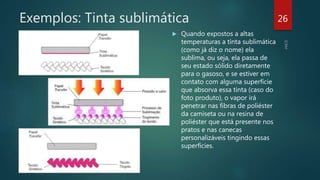
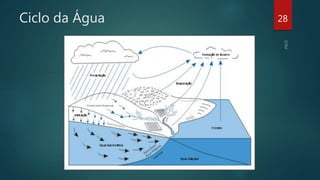
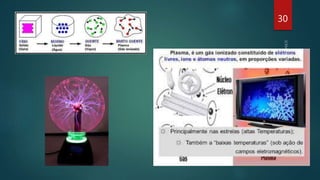
O documento aborda os estados físicos da matéria, explicando que ela pode ser sólida, líquida ou gasosa, sendo as mudanças de estado determinadas pela temperatura e pressão. Ele também discute como as substâncias mudam de estado físico e apresenta exemplos, como água e gás, além de mencionar o estado de plasma como o mais comum no universo. Técnicas para induzir mudanças de estado, como a utilização de panelas de pressão, também são exploradas.