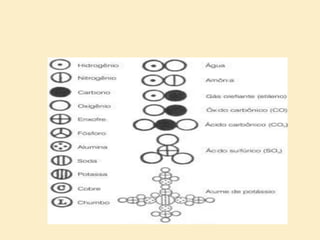
O documento descreve a vida e as contribuições científicas de John Dalton. Ele desenvolveu a teoria atômica moderna, proposta que inclui que toda matéria é composta de átomos indivisíveis e que os átomos de cada elemento têm massas características. Dalton também formulou a lei das proporções definidas e múltiplas, que estabelece como os elementos se combinam quimicamente.