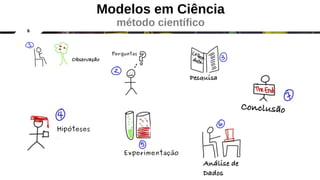
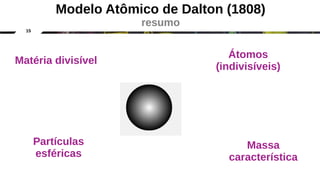
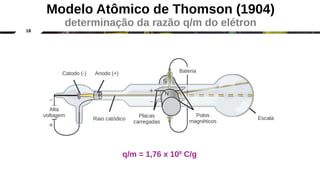
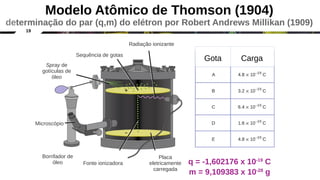
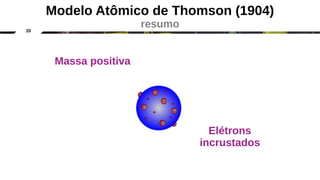
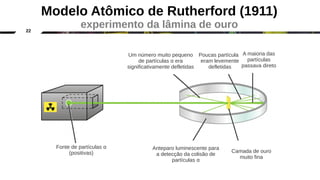
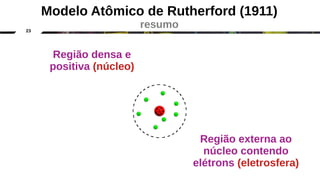
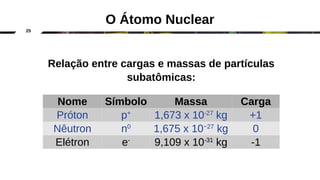
O documento discute a evolução dos modelos atômicos clássicos, começando com o modelo de Dalton no século 19 e evoluindo para os modelos de Thomson, Rutherford e Chadwick que identificaram as partículas subatômicas como prótons, elétrons e nêutrons e estabeleceram a estrutura nuclear do átomo.