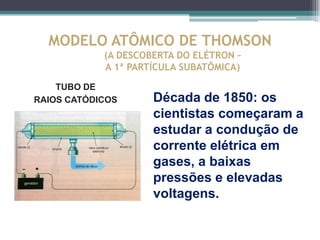
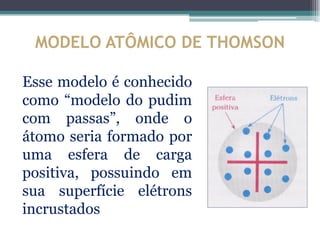
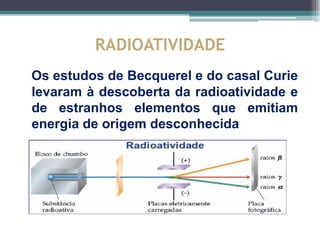
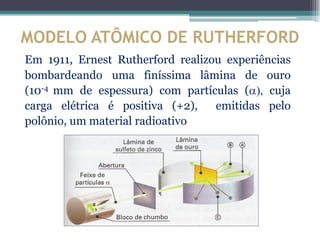
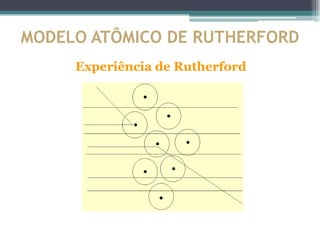
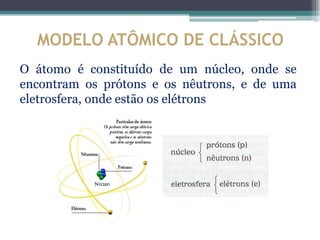
O documento descreve a evolução dos modelos atômicos ao longo do tempo, começando pelos filósofos gregos Leucipo e Demócrito no século V a.C. que propuseram a teoria de que a matéria era constituída por minúsculas partículas chamadas átomos. Posteriormente, cientistas como Dalton, Thomson, Rutherford e Chadwick contribuíram para os modelos atômicos através de experimentos que levaram à descoberta de novas partículas subatômicas como elétrons, pró