O documento apresenta uma série de questões relacionadas a características da água, escovas progressivas, separação de misturas e experimentos químicos. Também aborda a produção de soro de leite, interação dos alimentos com o ambiente e compostos orgânicos. Cada questão implica na análise de conhecimentos químicos e físicas, solicitando a escolha de alternativas corretas.












![35
a) O balão que murchou foi colocado em água quente, pois
o aumento da temperatura causou uma contração dos
gases da bexiga.
b) O balão que ficou mais cheio foi colocado em água
quente, devido ao aumento da temperatura do sistema e
à expansão dos gases presentes na bexiga.
c) O volume do balão que foi colocado em água fria
diminuiu, porque a pressão do sistema aumentou,
reduzindo o choque das partículas de gás com as paredes
do balão.
d) Em qualquer um dos casos, o volume dos balões foi
alterado, porque o tamanho das partículas de gás foi
modificado.
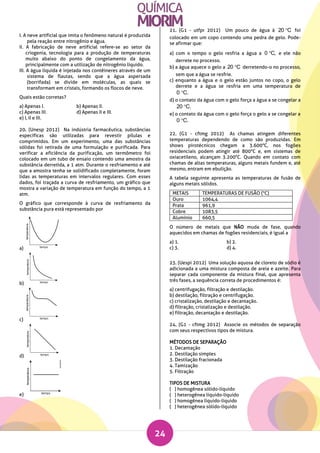
75. (G1 - ifce 2011) Em um laboratório, foram encontrados
dois frascos, I e II, cujas etiquetas apresentam informações
dos respectivos reagentes, conforme mostrado abaixo.
Com relação aos frascos, é correto afirmar-se que
a) por apresentarem as mesmas fórmulas moleculares,
esses compostos devem ser considerados formas
alotrópicas da matéria.
b) a atomicidade de uma substância está relacionada à
quantidade de átomos de um elemento presente no
material, assim a atomicidade do átomo de carbono,
presente nestas substâncias simples, corresponde a 4.
c) se fosse feita uma avaliação das propriedades
organolépticas destas substâncias, poderíamos, com toda
a convicção, proceder à identificação desses compostos.
d) se soubéssemos o volume ocupado por cada composto
nos respectivos recipientes e a quantidade de massa
contida em cada recipiente, seria possível
determinarmos as densidades específicas, que é uma
propriedade específica química destes materiais.
e) o que nos garante que estes materiais são realmente
diferentes é a propriedade física, o ponto de ebulição
exposta no rótulo dos recipientes.
76. (G1 - col.naval 2011) Segundo estudos conduzidos por
uma equipe multidisciplinar da UNICAMP (Universidade de
Campinas), o excesso de fluoreto (F) contido nas pastas
dentais comuns pode provocar em crianças, com idades
inferiores a 7 anos de idade, a fluorose, doença
caracterizada por manchas esbranquiçadas ou opacas nos
dentes em formação, devido à reação com a hidroxiapatita
[Ca10 (PO4) 6 (OH)2] , um sólido presente nas camadas
superficiais dos dentes, aumentando a porosidade nos
dentes, facilitando a quebra e o fingimento dos dentes, este
último pela absorção de corantes alimentícios.
De acordo com as informações fornecidas, qual propriedade
da matéria é comprometida pelo uso continuado de pastas
fluoretadas na faixa etária citada?
a) Elasticidade.
b) Inércia.
c) Tenacidade.
d) Extensão.
e) Massa.
77. (Uftm 2011) Em um béquer, sob agitação constante em
temperatura ambiente, são misturados 2 mL de solução
aquosa de NaC (d = 1,1 g/cm
3
), 2 mL de 4CC (d = 1,6
g/cm
3
) e 1 mL de 8 18C H (d = 0,7g/cm
3
).
Assinale a alternativa que melhor representa a distribuição
e a composição das fases líquidas no béquer após um
período adequado de repouso.
a)
b)
c)
d)
e)](https://image.slidesharecdn.com/lista1-2015-150305235717-conversion-gate01/85/Lista-1-2015-16-320.jpg)



![39
94. (Ita 2002) A adição de glicose sólida (C6H12O6) a clorato
de potássio (KCℓO3) fundido, a 400
°
C, resulta em um reação
que forma dois produtos gasosos e um sólido cristalino.
Quando os produtos gasosos formados nessa reação, e
resfriados à temperatura ambiente, são borbulhados em
uma solução aquosa 0,1mol/L em hidróxido de sódio,
contendo algumas gotas de fenolftaleína, verifica-se a
mudança de cor desta solução de rosa para incolor. O
produto sólido cristalino apresenta alta condutividade
elétrica, tanto no estado líquido como em solução aquosa.
Assinale a opção CORRETA que apresenta os produtos
formados na reação entre glicose e clorato de potássio:
a) CℓO2 (g), H2 (g), C (s).
b) CO2 (g), H2O (g), KCℓ (s).
c) CO (g), H2O (g), KCℓO4 (s).
d) CO (g), CH4 (g), KCℓO2 (s).
e) Cℓ2 (g), H2O (g), K2CO3 (s).
95. (Pucsp 2002) O clorato de potássio (KCℓO3) pode ser
decomposto por aquecimento, segundo a equação,
2 KCℓO3(s) 2 KCℓ(s) + 3 O2(g)
A decomposição de 2,45g de uma amostra contendo KCℓO3
produziu 0,72g de O2. Considerando que a reação foi
completa e que somente o KCℓO3 reagiu sob o
aquecimento, essa amostra contém
a) 100% de KCℓO3.
b) 90% de KCℓO3.
c) 75% de KCℓO3.
d) 60% de KCℓO3.
e) 30% de KCℓO3.
96. (Unesp 2002) Numa viagem, um carro consome 10kg de
gasolina. Na combustão completa deste combustível, na
condição de temperatura do motor, formam-se apenas
compostos gasosos. Considerando-se o total de compostos
formados, pode-se afirmar que os mesmos
a) não têm massa.
b) pesam exatamente 10kg.
c) pesam mais que 10kg.
d) pesam menos que 10kg.
e) são constituídos por massas iguais de água e gás
carbônico.
97. (Ufv 2002) Arseneto de gálio (GaAs) é um semicondutor
usado em lasers para leitoras de CDs. Um vendedor
ofereceu um lote de arseneto de gálio a uma indústria por
um preço muito bom. Antes de adquiri-lo, o químico
responsável pegou uma amostra do arseneto de gálio
comercial e determinou as percentagens (em massa) de
arsênio e de gálio, encontrando, respectivamente, 48,5% e
48,2% (m/m). Qual foi o parecer do químico sobre a
qualidade da amostra?
a) A amostra contém somente arseneto de gálio.
b) A amostra contém quantidades iguais de arsênio e de
gálio.
c) A amostra contém duas vezes mais gálio do que arsênio.
d) A amostra contém mais arsênio do que deveria se
estivesse pura.
e) A amostra contém algum outro ânion além do arseneto.
98. (Ufmg 2002) A análise elementar de um
hidrocarboneto X pode ser feita por meio da reação de
oxidação, conforme a equação
X(s)+45CuO(s) 15CO2(g)+15H2O(ℓ)+45Cu(s)
Assim sendo, é CORRETO afirmar que, para o
hidrocarboneto X, a proporção entre átomos de carbono e
átomos de hidrogênio, NESSA ORDEM, é de
a) 1 : 1. b) 1 : 2.
c) 1 : 3. d) 2 : 3.
99. (Pucmg 2001) Considere as seguintes proposições:
I. Não existe sistema polifásico formado de vários gases ou
vapores.
II. A água é uma mistura de hidrogênio e oxigênio.
III. Todo sistema homogêneo é uma mistura homogênea.
IV. Existe sistema monofásico formado por vários sólidos.
V. Todo sistema polifásico é uma mistura heterogênea.
São VERDADEIRAS as afirmações:
a) I, II e III b) I e II apenas
c) I e IV apenas d) III, IV e V
100. (Unesp 2000) São colocadas para reagir entre si as
massas de 1,00g de sódio metálico e 1,00g de cloro gasoso.
Considere que o rendimento da reação é 100%. São dadas
as massas molares, em g/mol: Na=23,0 e Cℓ=35,5. A
afirmação correta é:
a) há excesso de 0,153 g de sódio metálico.
b) há excesso de 0,352 g de sódio metálico.
c) há excesso de 0,282 g de cloro gasoso.
d) há excesso de 0,153 g de cloro gasoso.
e) nenhum dos dois elementos está em excesso.
Gabarito:
1: [B] 2: [B] [3: [A]4: [E] 5: [E] 6: [A] 7: [B]8: [A]9: [E]10: [D]
11: [C]12: [D] 13: [E] 14: [C]15: [D]16: [E]17: [C]18: [A]19: [B]
20:[C]21:[C]22:[C]23:[E]24:[B]25:[D]26:[C]27:[C]28:[D]29:[E]
30:[A]31:[D]32:[D]33:[C]34:[D]35:[B]36:[D]37: [A] 38: [C]
39:[E]40:[D]41:[B]42: [C]43:[D]44:[D]45:[A]46: [D] 47: [C]
48: [E]49: [D]50: [C]51: [B]52: [C] 53: [B]54: [A]55: [C] 56: [A]
57: [D] 58:[C]59:[E]60: [C]61: [D]62:[D]63:[E]64:[C]65: [A]
66: [C] 67:[C]68:[D]69:[B]70:[B]71:[B]72: [A]73: [B]74: [B]
75: [E]76:[C]77:[C] 78:[A]79:[D]80: [A]81:[C] 82:[A]83: [A]
84: [A] 85: [A] 86: [E] 87: [A] 88: [D] 89: [C] 90: [A] 91: [D]
92: [C] 93: [C] 94: [B] 95: [C] 96: [C] 97: [E] 98: [B] 99: [C]
100: [B]](https://image.slidesharecdn.com/lista1-2015-150305235717-conversion-gate01/85/Lista-1-2015-20-320.jpg)
