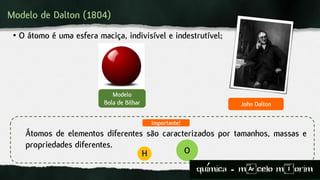
O documento descreve a evolução dos modelos atômicos desde a Grécia Antiga até o final do século XIX. Começa com os filósofos gregos Leucipo e Demócrito, que desenvolveram a teoria atomista de que a matéria é constituída de átomos indivisíveis. Posteriormente, John Dalton formulou a teoria atômica moderna no início do século XIX. Finalmente, com o advento da eletricidade no século XIX, J.J. Thomson propôs um novo modelo atômico para explicar os fenô