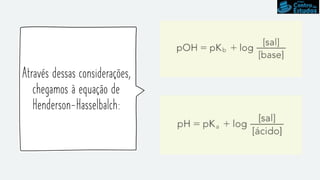
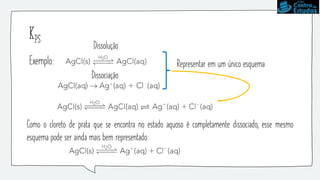
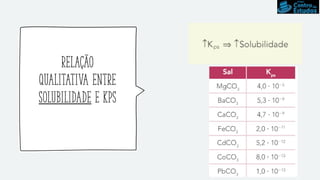
O documento discute conceitos sobre hidrólise salina, soluções tampão e produto de solubilidade (Kps). Explica que a hidrólise salina depende se o sal é derivado de uma base forte ou fraca e de um ácido forte ou fraco, e que isso determina se o pH aumenta, diminui ou permanece neutro. Também descreve como soluções tampão mantêm o pH constante e como calcular o pH usando a equação de Henderson-Hasselbalch. Finalmente, discute a relação entre Kps e a solubilidade de substân