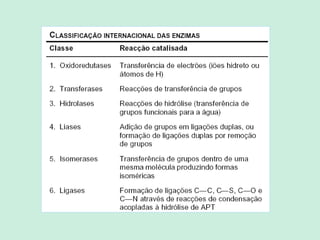
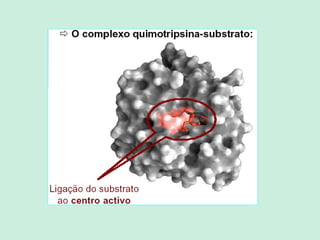
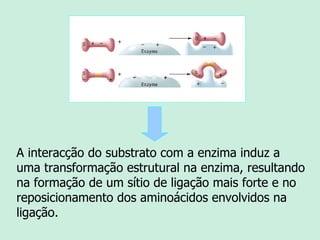
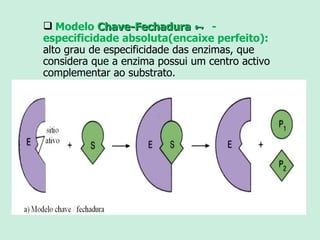
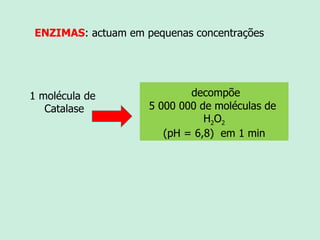
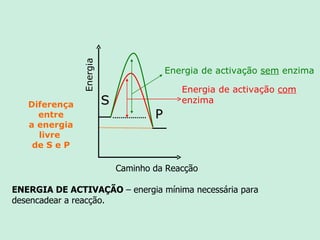
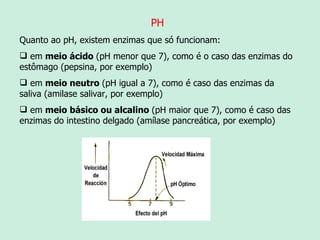
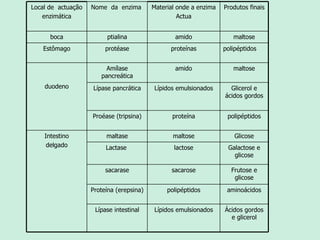
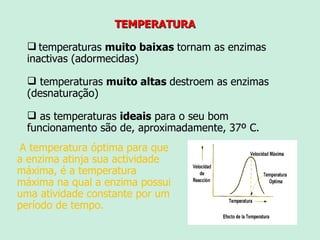
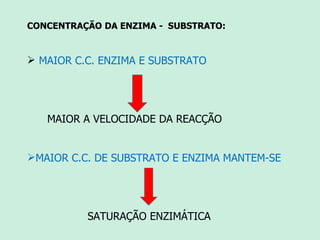
O documento descreve as propriedades e funções das enzimas. As enzimas são proteínas que aceleram as reações químicas no corpo sem alterar os equilíbrios das reações. As enzimas atuam de forma específica, eficiente e em pequenas quantidades, e são influenciadas por fatores como pH, temperatura e concentração de substrato. As enzimas têm muitas aplicações importantes na indústria alimentícia, de rações, couro, têxtil e de limpeza.