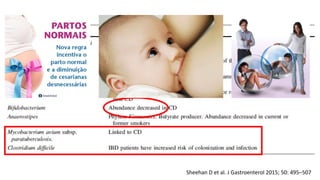
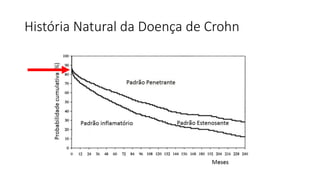
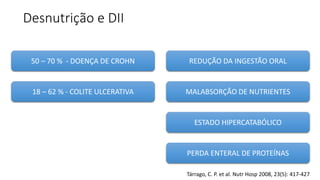
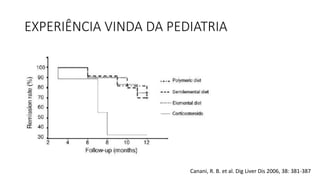
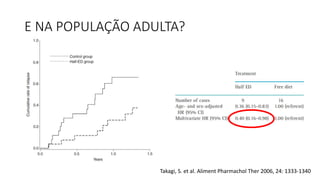
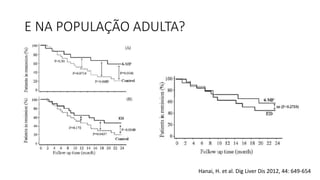
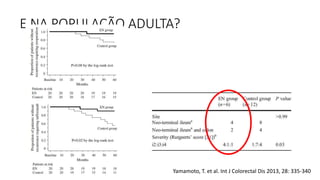
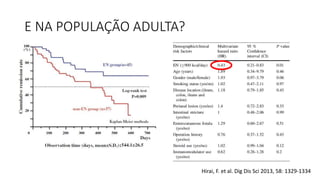
O documento discute o tratamento nutricional de doenças inflamatórias intestinais. A terapia nutricional pode ser usada como tratamento primário ou suplementar e tem benefícios como melhorar o crescimento e cicatrização da mucosa. Estudos em adultos sugerem que a nutrição enteral pode auxiliar na indução de remissão, especialmente em pacientes com doença de Crohn de padrão inflamatório não-estenso.