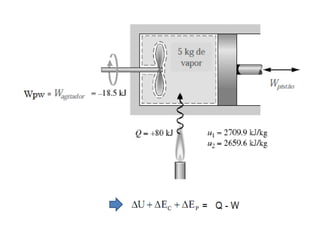
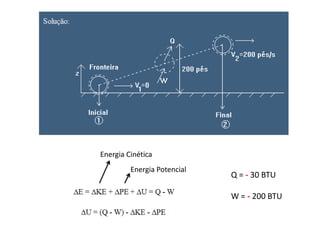
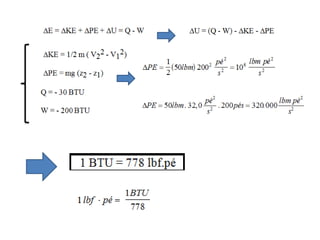
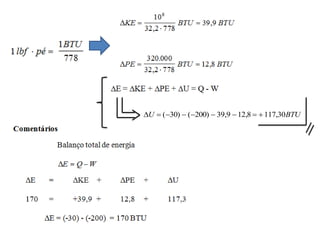
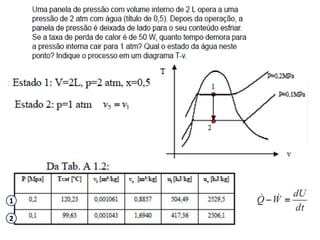
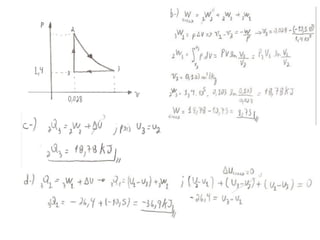
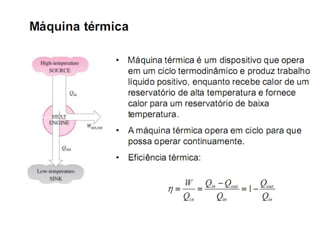
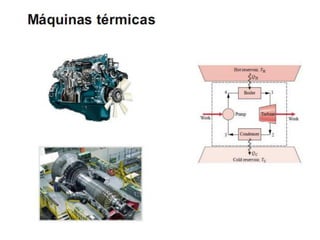
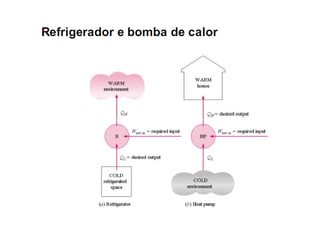
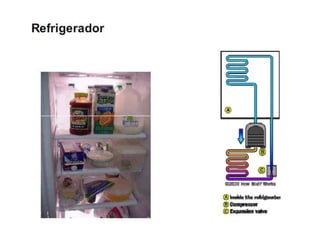
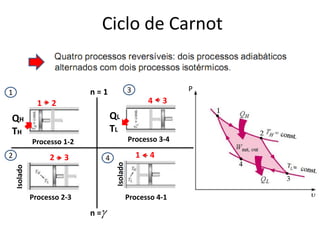
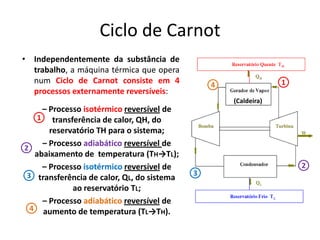
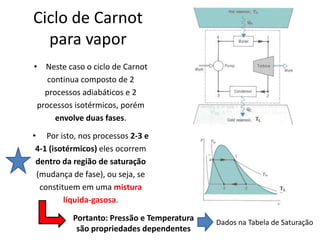
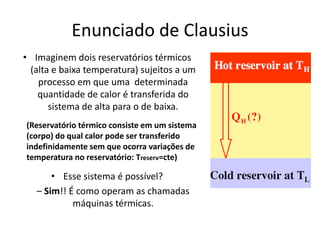
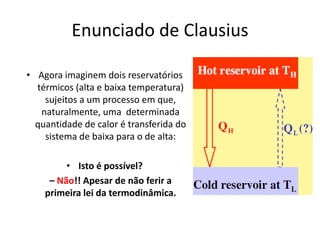
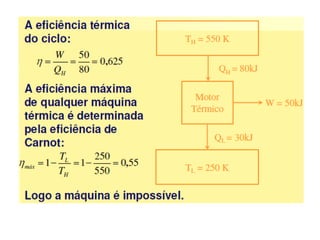
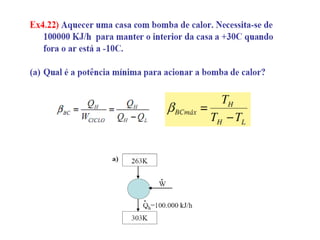
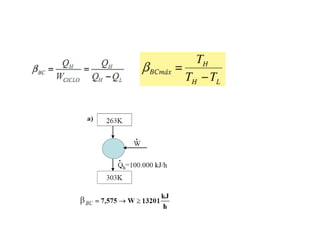
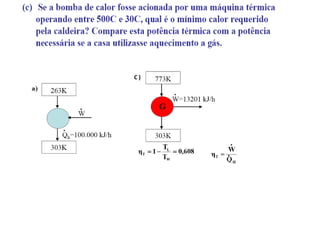
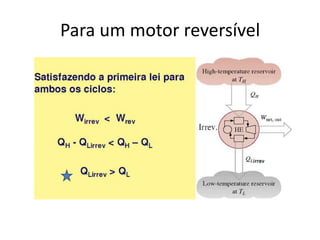
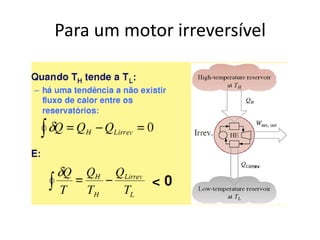
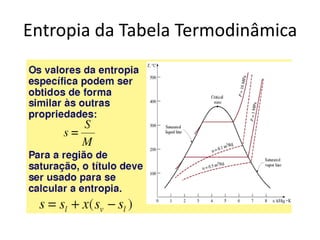
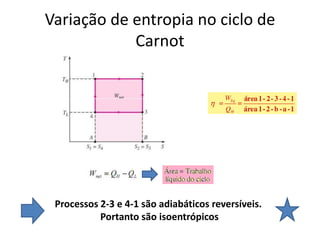
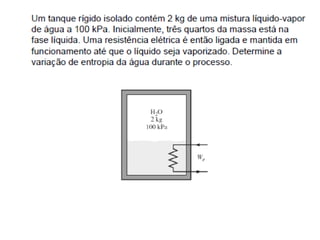
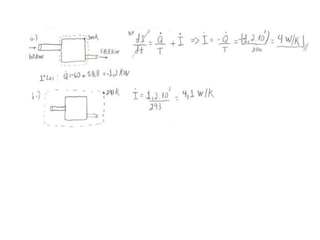
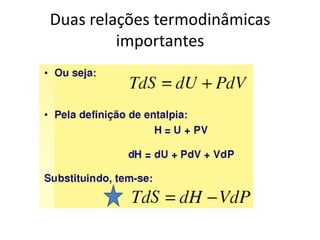
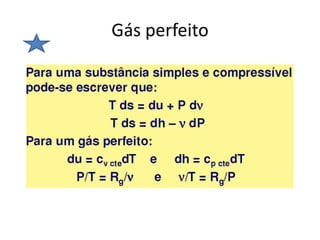
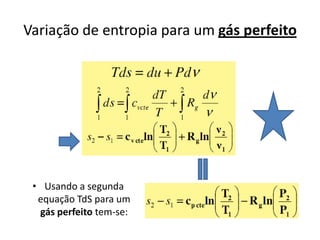
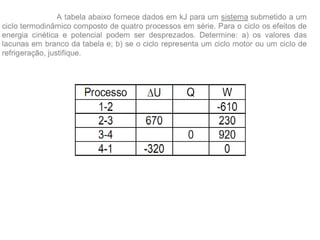
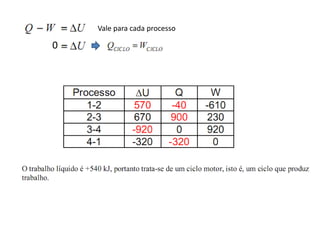
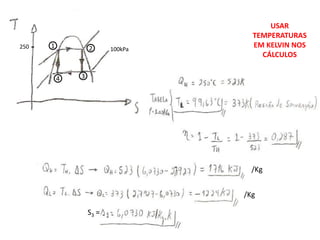
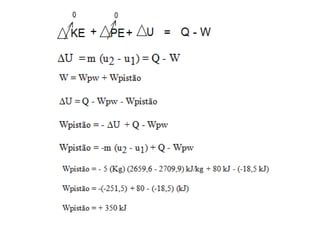Este documento resume os principais pontos da primeira e segunda lei da termodinâmica, incluindo: a primeira lei trata da conservação de energia em sistemas termodinâmicos, enquanto a segunda lei estabelece que o calor não flui naturalmente de um corpo frio para um quente. O documento também discute processos reversíveis, o ciclo de Carnot, eficácia máxima de máquinas térmicas e a escala Kelvin de temperatura.