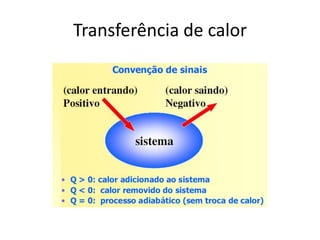
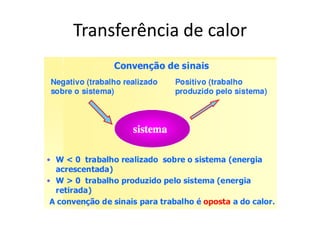
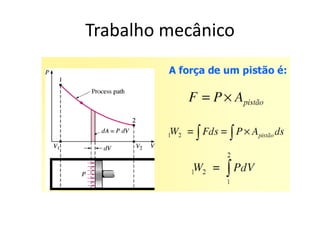
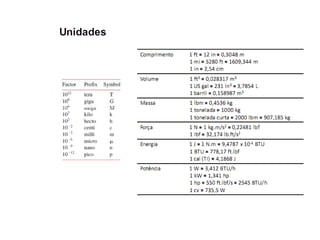
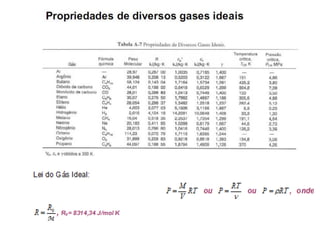
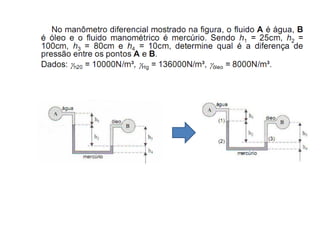
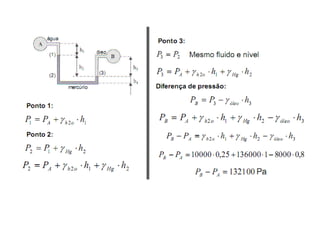
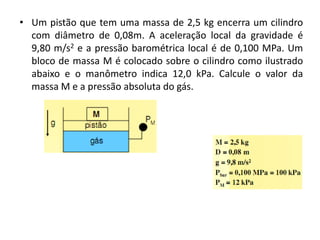
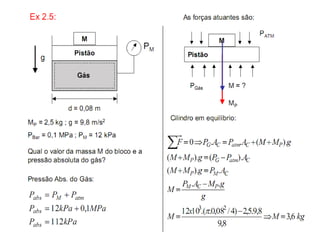
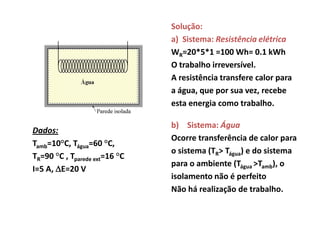
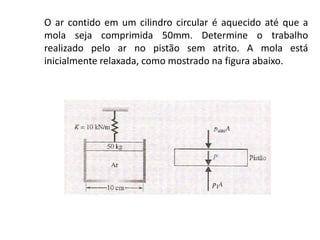
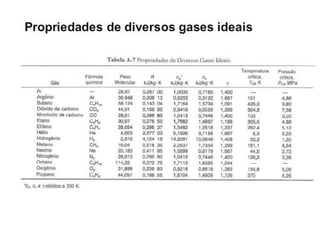
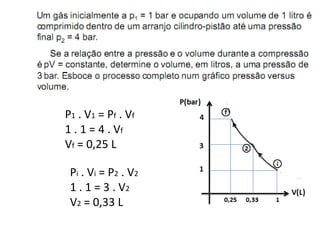
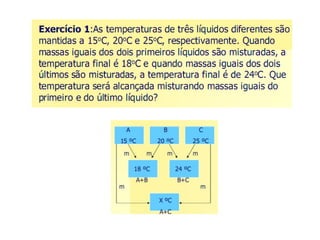
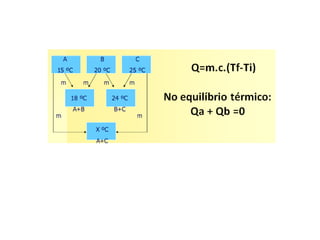
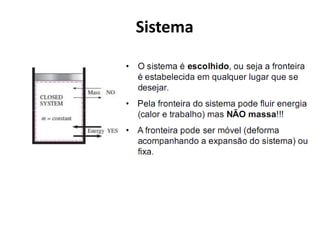
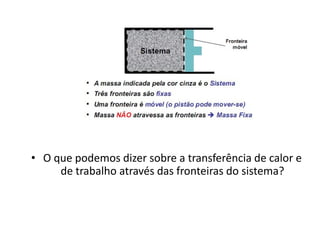
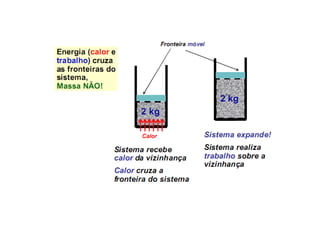
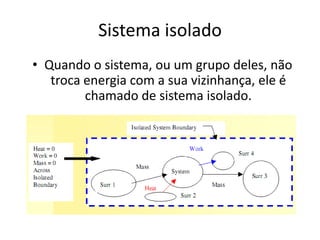
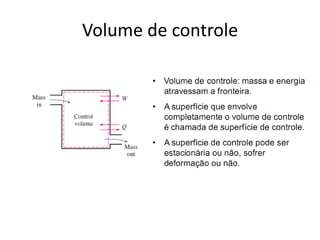
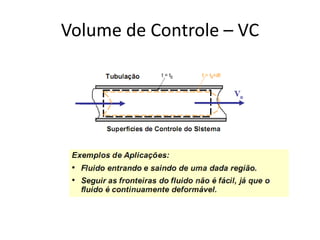
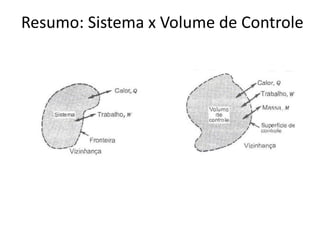
O documento apresenta conceitos termodinâmicos como sistema, propriedades termodinâmicas, equilíbrio termodinâmico e processos reversíveis. Discute a diferença entre sistema termodinâmico e volume de controle e explica como calor e trabalho podem ser transferidos através de suas fronteiras.










![Temperatura
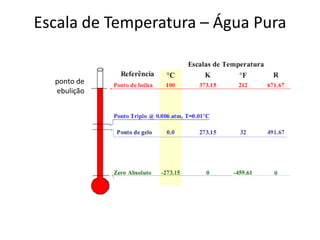
• Existem duas escalas de temperatura: Relativa e Absoluta
• Escala relativa:
− É a que comumente conhecemos (Celsius e Fahrenheit).
• Escala absoluta:
− Trabalha-se em Kelvin.
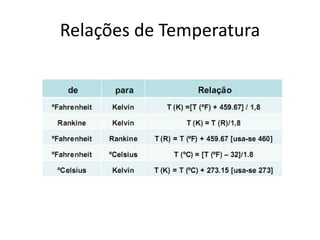
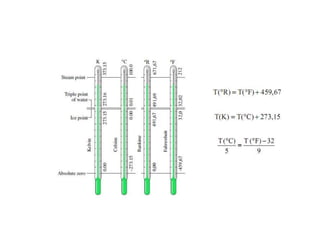
• Relação entre unidades:
− T (R) = T (ºF) + 459,67 *arredondado 460]
− T (K) = T (ºC) + 273,15 *arredondado 273]](https://image.slidesharecdn.com/captulo2-110816133502-phpapp02/85/Capitulo-2-0-22-320.jpg)