O documento discute conceitos fundamentais da termodinâmica, incluindo:
1) Energia interna é a soma das energias cinéticas e potenciais das partículas de um corpo;
2) A energia interna de um gás perfeito depende apenas da temperatura, de acordo com a Lei de Joule;
3) O trabalho realizado em uma transformação gasosa depende da variação de volume e da pressão.


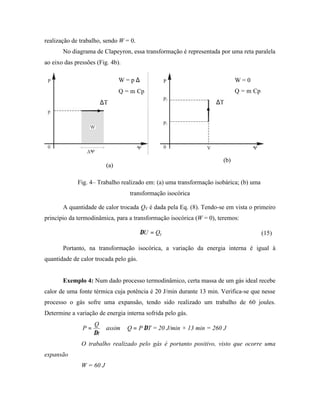
![W = p ∆∀
N 3
[ ]
m2 m = N × m = J (4)
A equação (4) é válida apenas para transformações isobáricas, ou seja, a pressão
constante.
O trabalho realizado no processo isobárico tem o sinal da variação do volume ∆∀,
visto que p é uma grandeza sempre positiva.
Na expansão isobárica, isto é, quando o volume aumenta, temos:
∆∀ > 0 ⇒ W > 0 (5)
Neste caso, dizemos que o gás realizou trabalho, o que representa uma perda de
energia para o ambiente.
Se o gás sofrer uma compressão isobárica, isto é, se o volume diminuir, teremos
∆∀ < 0 ⇒ W < 0 (6)
Portanto o ambiente é que realizou trabalho sobre o gás, o que representa para o gás
um ganho de energia do ambiente.
Podemos representar esta transformação em um sistema de eixos cartesianos, em
que se representa em ordenadas a pressão e em abscissas o volume (diagrama de
Clapeyron), a transformação isobárica é representada por uma reta paralela ao eixo dos
volumes (Fig. 2a). Este gráfico tem uma importante propriedade: a área da figura
compreendida entre a reta representativa e o eixo dos volumes mede numericamente o
módulo do trabalho realizado na transformação. Sendo a área do retângulo individualizado
na Fig. 2a o trabalho realizado no processo:](https://image.slidesharecdn.com/capitulo4-120907010801-phpapp02/85/Apostila-de-termodinamica-Cap-4-3-320.jpg)