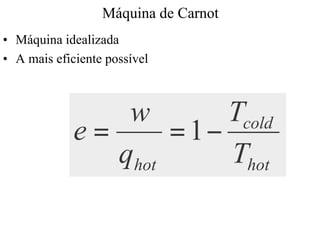
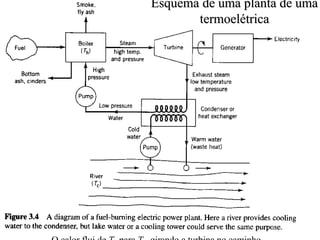
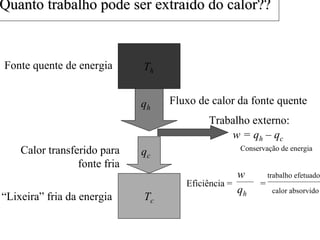
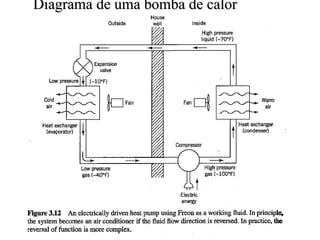
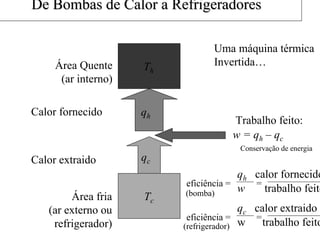
O documento discute máquinas térmicas e refrigeradores, explicando que calor pode ser transformado em trabalho mecânico através destes dispositivos. Apresenta o conceito de máquina térmica e como funciona, discutindo também o princípio de Carnot e os limites de eficiência impostos pela segunda lei da termodinâmica. Explica como bombas de calor e refrigeradores são máquinas térmicas operando de forma inversa.


















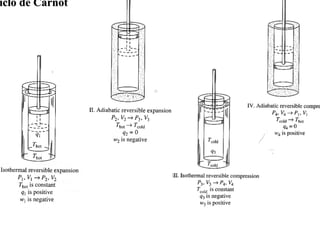

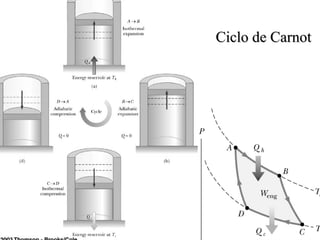
![Análise do Ciclo de Carnot……
A soma de todos os qi para todos os passos é diferente de zero; entretanto, a soma das
expressões qrev/T é zero.
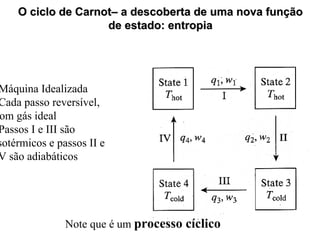
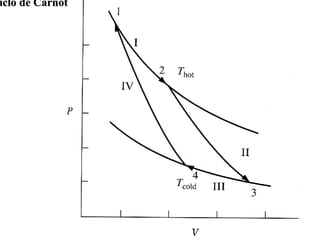
Passo I :?dqrev/T = 1/Thot ?dqrev = q1/ Thot
Passo III: ?dqrev/T = 1/Tcold ?dqrev = q3/ Tcold
Passos II e IV, dqrev é zero (adiabático).Portanto:
?dqrev/T = 0
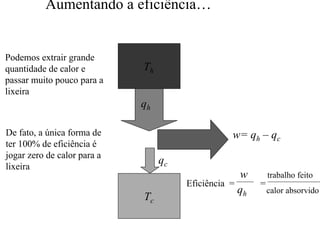
Para o ciclo inteiro temos q = -w
q1/ Thot+ q3/ Tcold = nR ln V2/V3 + nR ln V4/V1 = nR ln [V2V4/V3V1] = 0](https://image.slidesharecdn.com/termodinamica2aleiaula3-141119175013-conversion-gate02/85/Termodinamica-2a-lei_aula3-31-320.jpg)