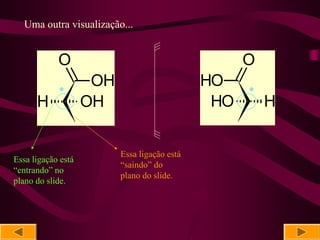
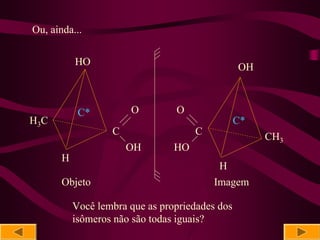
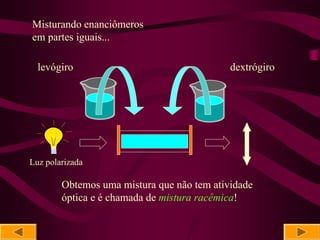
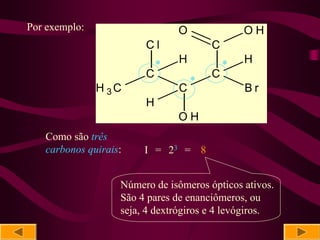
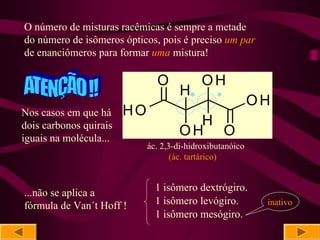
O documento discute isomeria óptica, especificamente sobre enantiômeros. 1) Enantiômeros são isômeros ópticos que são imagens não superponíveis um do outro e podem ser dextrógiros ou levógiros. 2) A presença de pelo menos um carbono quiral é necessária para uma molécula ser ópticamente ativa. 3) O número de isômeros ópticos é calculado pela fórmula de Van't Hoff, I = 2n, onde n é o número de carbonos quirais.