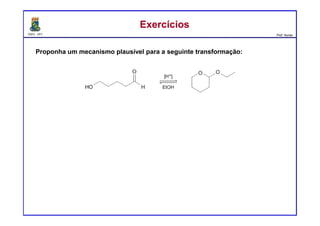
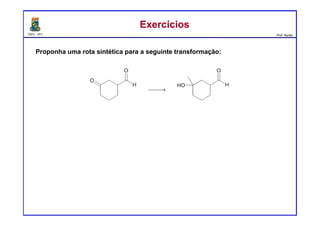
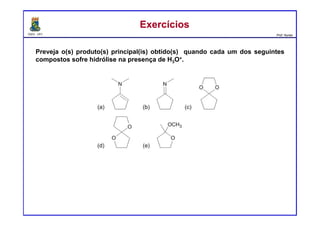
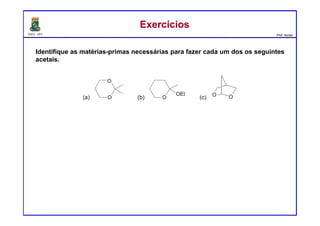
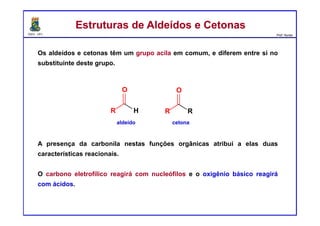
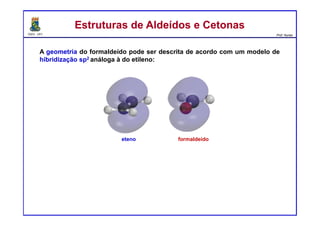
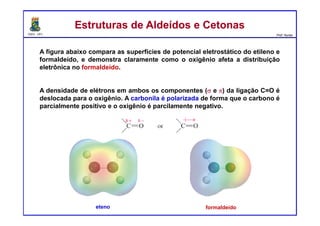
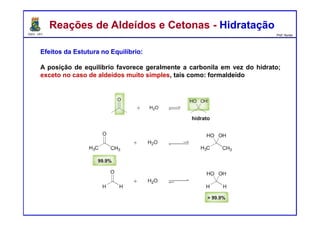
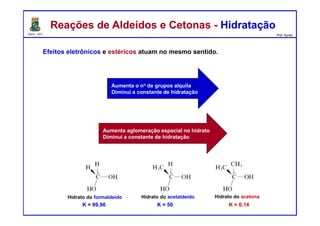
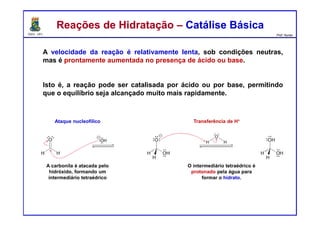
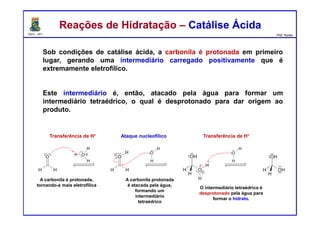
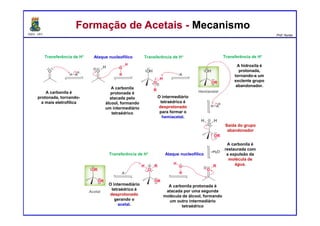
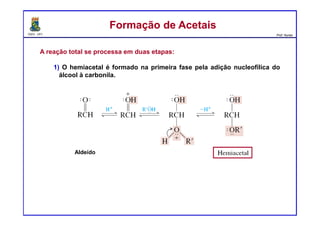
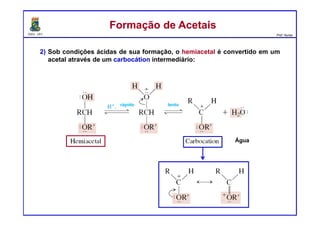
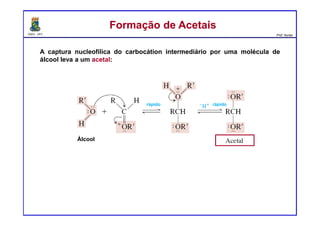
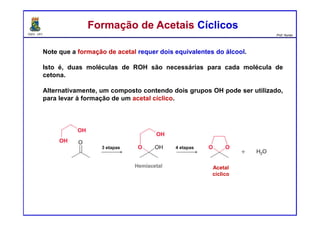
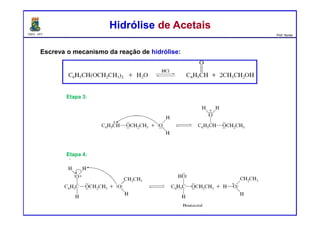
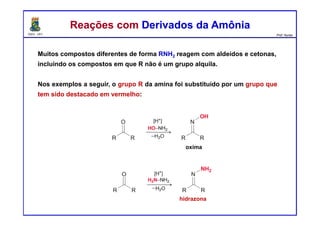
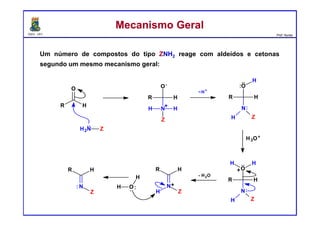
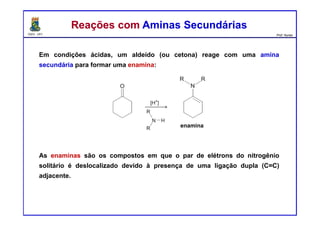
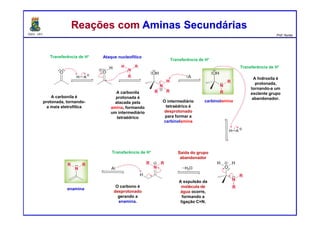
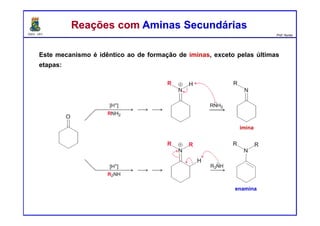
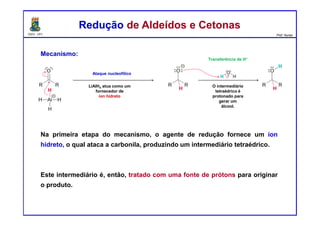
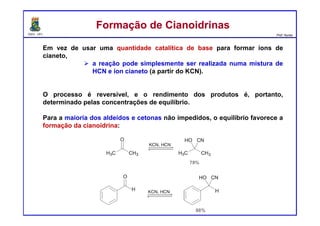
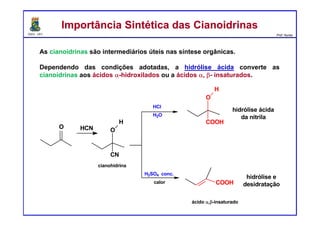
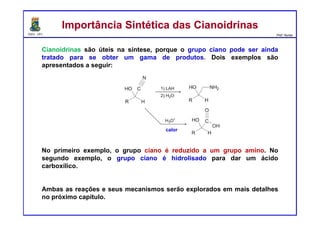
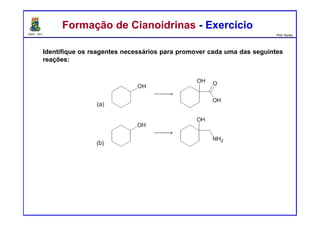
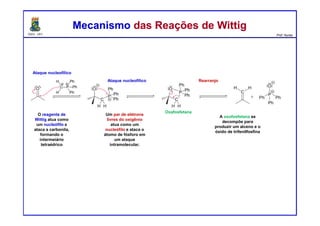
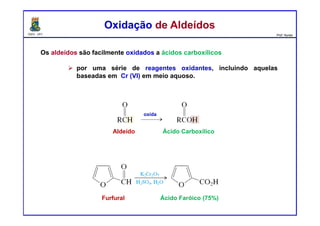
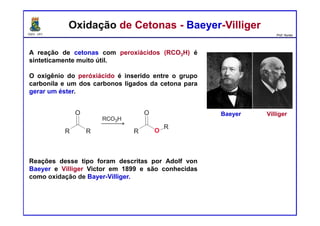
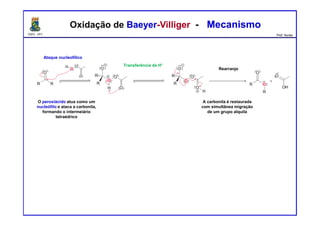
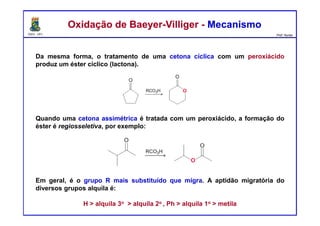
O documento descreve reações de aldeídos e cetonas, incluindo suas estruturas, propriedades e reações de hidratação e formação de acetais. Grupos alquila estabilizam a ligação carbonila enquanto grupos eletroretiradores a desestabilizam, afetando as constantes de equilíbrio. A hidratação é mais favorável para aldeídos simples e menos favorável para cetonas com mais grupos alquila devido aos efeitos eletrônicos e estéricos. A formação de acetais envolve































![DQOI - UFC Prof. Nunes
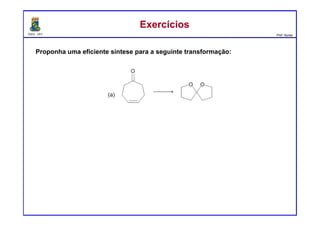
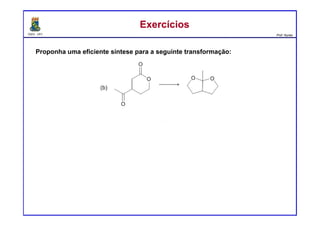
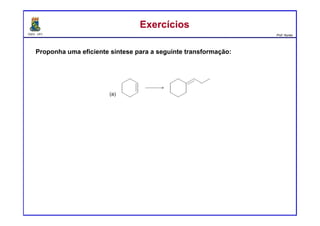
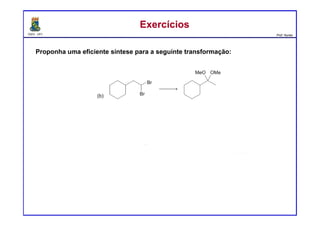
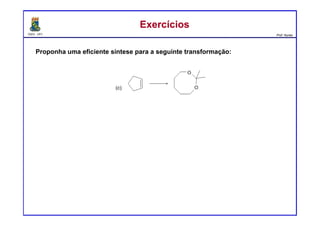
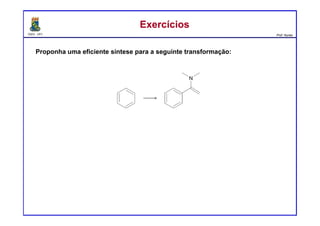
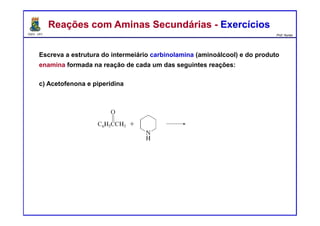
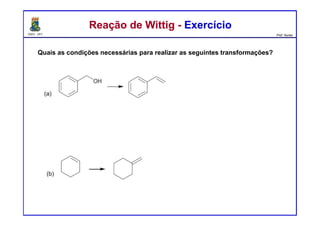
ExercíciosExercícios
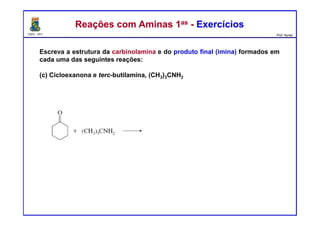
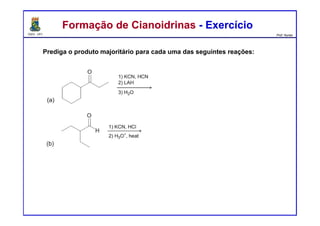
Preveja o(s) principal(is) produto(s) formados a partir do tratamento da acetona
com os compostos seguintes reagentes:
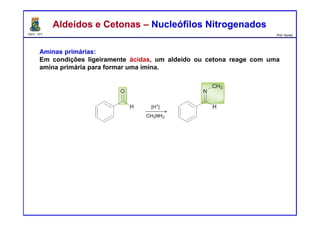
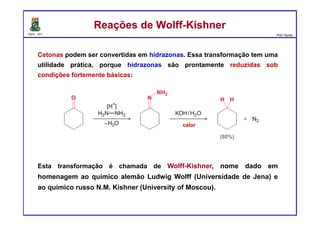
(a) [H+], NH3, (-H2O)
(b) [H+], CH3NH2, (-H2O)
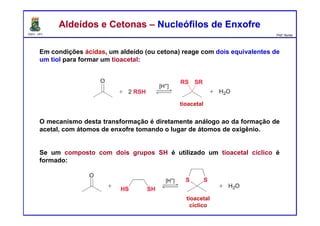
(c) [H+], excesso de EtOH, (-H2O)
(d) [H+], (CH3)2NH, (-H2O)
(e) [H+], NH2NH2, (-H2O)
(f) [H+], NH2OH, (-H2O)
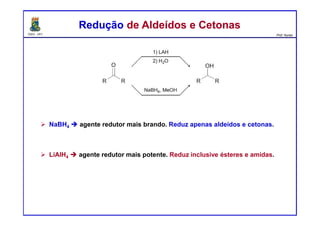
(g) NaBH4, MeOH
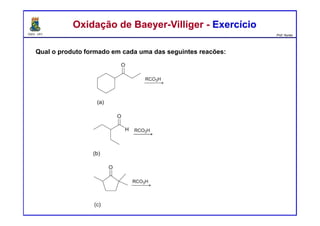
(h) Ácido metacloroperbenzóico
(i) HCN, KCN
(j) EtMgBr seguido por H2O
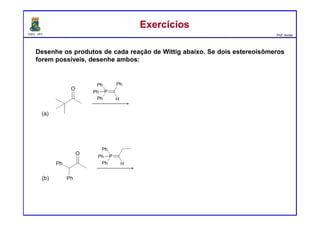
(k) (C6H5)3P=CHCH2CH3
(l) (l) LiAlH4 seguido por H2O](https://image.slidesharecdn.com/unidade062011-110528144153-phpapp01/85/Reacoes-de-Aldeidos-e-Cetonas-90-320.jpg)