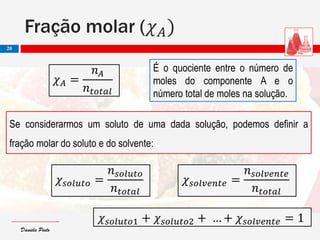
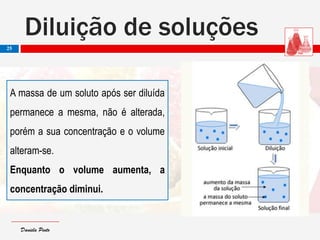
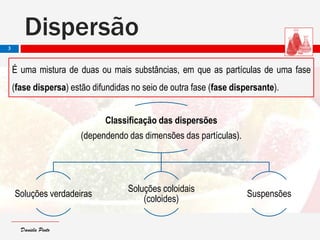
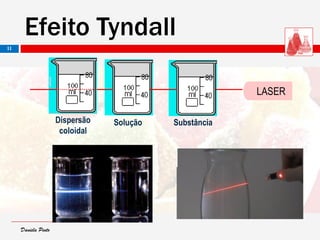
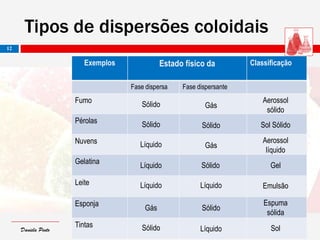
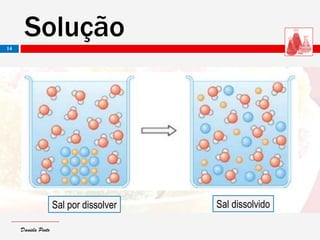
O documento descreve as características de dispersões, soluções, colóides e suspensões. Distingue-se entre elas com base no tamanho das partículas dispersas: soluções têm partículas menores que 1 nm; colóides entre 1 nm e 1000 nm; e suspensões maiores que 1000 nm. Também aborda conceitos como concentração, diluição e exemplos de diferentes tipos de dispersões.










![Daniela PintoDaniela Pinto
Concentração mássica
15
Massa de Soluto
[kg]
Volume de solução
[m3]
[dm3]Concentração mássica
[kg m-3]
[g cm-3]
[g dm-3]
𝐶 𝑚 =
𝑚
𝑉
Indica a massa de soluto existente em
cada uma unidade de volume da
solução.
SI](https://image.slidesharecdn.com/14-dispersoesecomposicaoquantitativadesolucoes-150126155041-conversion-gate02/85/14-dispersoes-e-composicao-quantitativa-de-solucoes-15-320.jpg)
![Daniela PintoDaniela Pinto
Concentração molar ou Molaridade
16
Quantidade química de soluto
[mol]
Volume de solução
[m3]
[dm3]Concentração molar
[mol m-3]
[mol dm-3]
𝐶 =
𝑛
𝑉
Indica a quantidade química de soluto
(mol) por unidade de volume da
solução.
SI](https://image.slidesharecdn.com/14-dispersoesecomposicaoquantitativadesolucoes-150126155041-conversion-gate02/85/14-dispersoes-e-composicao-quantitativa-de-solucoes-16-320.jpg)