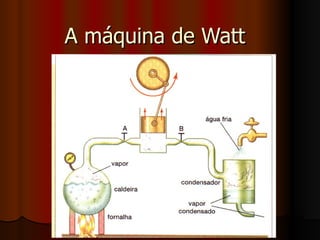
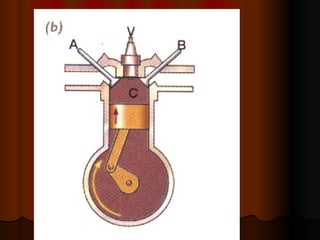
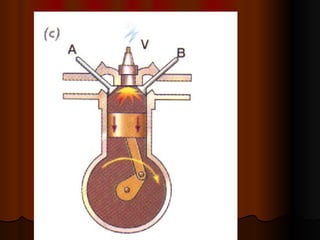
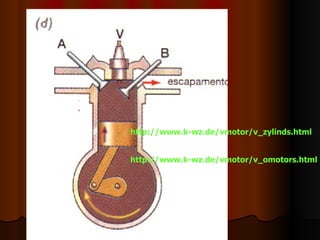
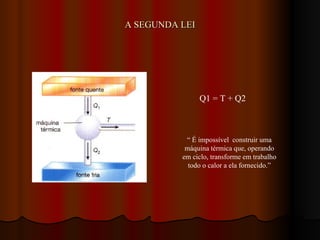
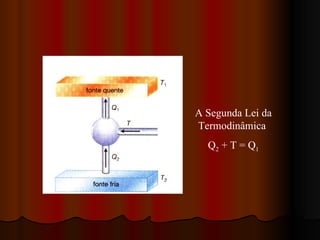
O documento explica a Segunda Lei da Termodinâmica, que afirma que a quantidade de trabalho útil que pode ser obtido de energia no universo está diminuindo constantemente à medida que o universo tende ao equilíbrio térmico. Discute como máquinas térmicas como motores a vapor e de explosão funcionam de acordo com essa lei, transformando apenas parte da energia térmica em trabalho mecânico.


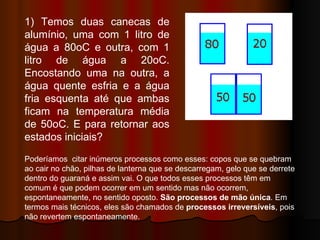


![A Segunda Lei da Termodinâmica afirma que a quantidade de trabalho útil que você pode obter a partir da energia do universo está constantemente diminuindo. Quando se tem uma grande porção de energia num “lugar”, tem-se alta temperatura aqui e baixa temperatura lá, então pode-se obter trabalho dessa situação. Quanto menor for a diferença de temperatura, menos trabalho você pode obter. Então, de acordo com a Segunda Lei da Termodinâmica, há sempre uma tendência para as áreas quentes se resfriarem e as áreas frias se aquecerem - assim cada vez menos trabalho poderá ser obtido. Até que finalmente, quando tudo estiver numa mesma temperatura, você não poderá mais obter nenhum trabalho disso, mesmo que toda a energia continue lá. E isso é verdade para TUDO em geral, em todo o universo.“ [Isaac Asimov in The Origin of the Universe in the ORIGINS: How the World Came to Be video series 5299 USA: Eden Communications, 1983).]](https://image.slidesharecdn.com/segundaleidatermodinmica-091024122531-phpapp01/85/Segunda-Lei-Da-TermodinaMica-6-320.jpg)