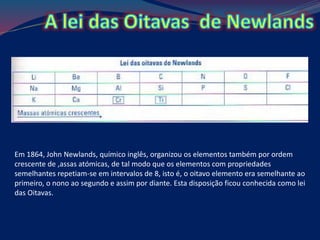
A tabela periódica foi originalmente criada em 1789 por Antoine Lavoisier e divide os elementos químicos em grupos e períodos com base em suas propriedades. Ao longo dos séculos, químicos como Dobereiner, Newlands e Mendeleiev contribuíram para o desenvolvimento e organização da tabela periódica moderna, que está organizada por número atômico e ajuda a prever propriedades dos elementos.












![Porque razão a tabela é “ Periodica ” ?
- A tabela é chamada Tabela Periodica porque há propriedades dos atomos dos elementos
que se repetem periodicamente
De onde são derivados os nomes dos Elementos Químicos?
Muitos elementos são derivados da primeira letra [ex., H para Hidrogénio] ou das duas primeiras
letras [ex., He para Hélio] de seus nomes. Os seus nomes provêm do Latim.](https://image.slidesharecdn.com/trabalho-tabelaperiodica-140620162934-phpapp01/85/Trabalho-tabela-periodica-18-320.jpg)
