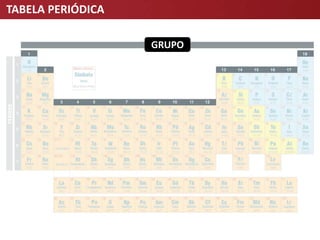
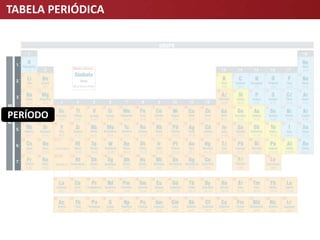
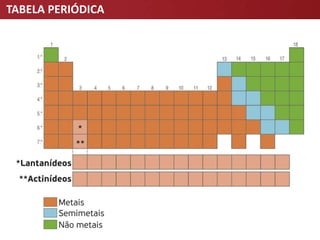
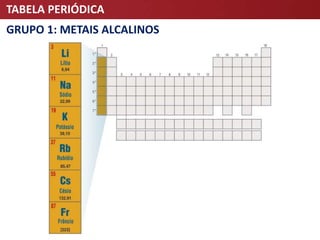
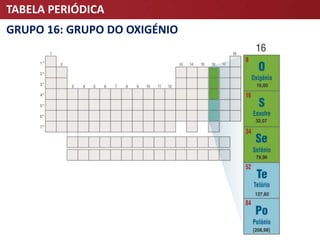
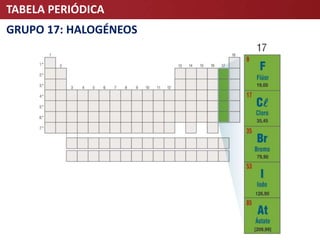
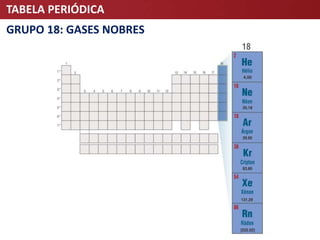
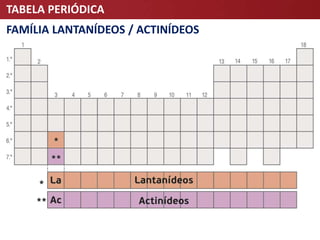
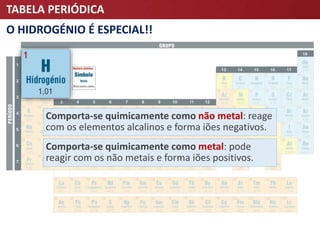
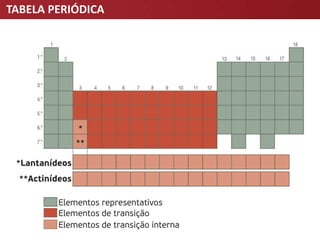
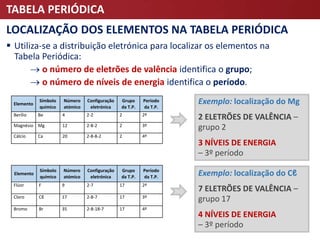
O documento descreve a evolução da Tabela Periódica dos Elementos Químicos, desde as primeiras tentativas de organização por Lavoisier e Döbereiner até à tabela moderna organizada por número atômico. Destaca contribuições-chave como as de Mendeleev e Meyer que estabeleceram a lei da periodicidade.