1) O documento descreve a evolução dos modelos atômicos ao longo da história, desde as ideias filosóficas de Aristóteles e Platão até o modelo atômico atual.
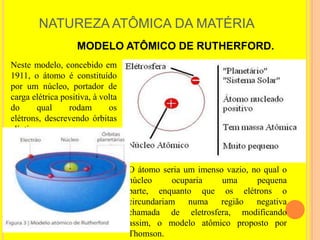
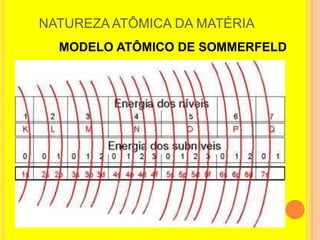
2) Inclui os principais modelos propostos por cientistas como Dalton, Thomson, Rutherford e Bohr e suas contribuições para entender a estrutura atômica.
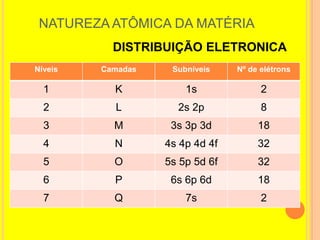
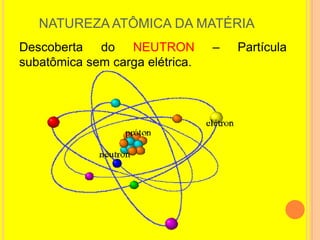
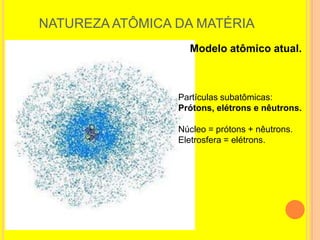
3) Atualmente sabe-se que os átomos são constituídos por prótons, nêutrons e elétrons organizados em um núcleo envolto por uma elet