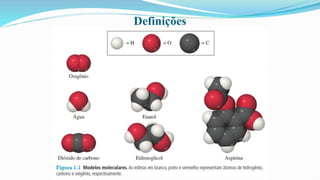
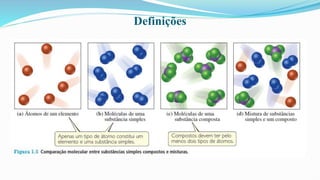
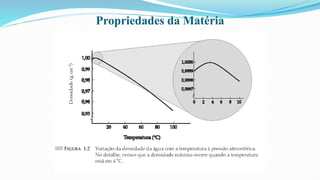
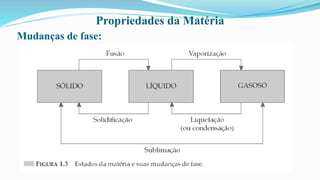
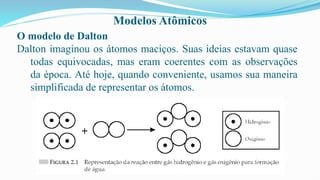
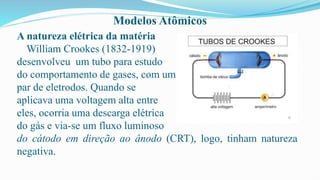
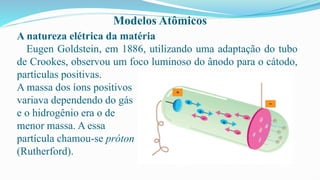
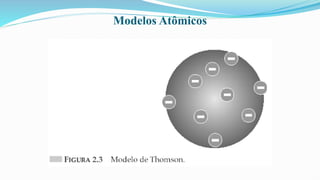
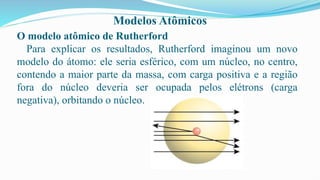
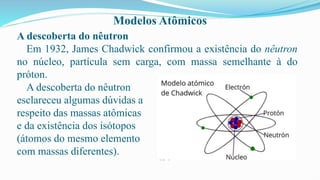
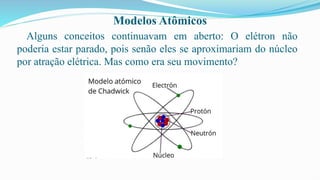
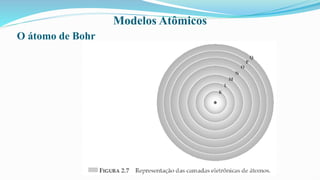
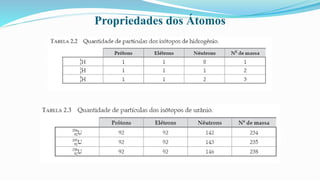
O documento fornece definições básicas sobre química, matéria, átomos, moléculas, compostos, misturas e propriedades da matéria. Explora os modelos atômicos de Dalton, Thomson, Rutherford e Bohr, culminando na descoberta do nêutron e na distribuição eletrônica por números quânticos.