Escola Estadual Minas Gerais Revisão de Conteúdo Química Soluções e Solubilidade
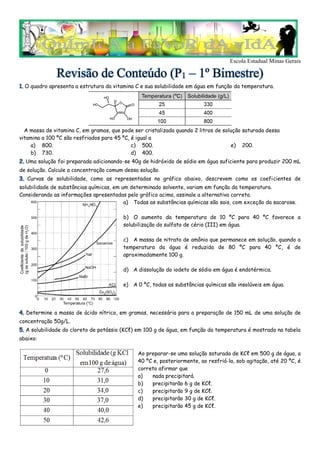
- 1. Escola Estadual Minas Gerais Revisão de Conteúdo (P1 – 1º Bimestre) 1. O quadro apresenta a estrutura da vitamina C e sua solubilidade em água em função da temperatura. A massa de vitamina C, em gramas, que pode ser cristalizada quando 2 litros de solução saturada dessa vitamina a 100 ºC são resfriados para 45 ºC, é igual a a) 800. b) 730. c) 500. d) 400. e) 200. 2. Uma solução foi preparada adicionando-se 40g de hidróxido de sódio em água suficiente para produzir 200 mL de solução. Calcule a concentração comum dessa solução. 3. Curvas de solubilidade, como as representadas no gráfico abaixo, descrevem como os coeficientes de solubilidade de substâncias químicas, em um determinado solvente, variam em função da temperatura. Considerando as informações apresentadas pelo gráfico acima, assinale a alternativa correta. a) Todas as substâncias químicas são sais, com exceção da sacarose. b) O aumento da temperatura de 10 ºC para 40 ºC favorece a solubilização do sulfato de cério (III) em água. c) A massa de nitrato de amônio que permanece em solução, quando a temperatura da água é reduzida de 80 ºC para 40 ºC, é de aproximadamente 100 g. d) A dissolução do iodeto de sódio em água é endotérmica. e) A 0 ºC, todas as substâncias químicas são insolúveis em água. 4. Determine a massa de ácido nítrico, em gramas, necessária para a preparação de 150 mL de uma solução de concentração 50g/L. 5. A solubilidade do cloreto de potássio (KCℓ) em 100 g de água, em função da temperatura é mostrada na tabela abaixo: Ao preparar-se uma solução saturada de KCℓ em 500 g de água, a 40 ºC e, posteriormente, ao resfriá-la, sob agitação, até 20 ºC, é correto afirmar que a) nada precipitará. b) precipitarão 6 g de KCℓ. c) precipitarão 9 g de KCℓ. d) precipitarão 30 g de KCℓ. e) precipitarão 45 g de KCℓ.
- 2. 6. (Mack-SP) Qual a concentração, em g/L, da solução obtida ao se dissolverem 4g de cloreto de sódio em 50 cm3 de solução? 7. Uma solução foi preparada a 30 ºC pela dissolução de 80 g de um sal inorgânico hipotético em 180 g de água. A solubilidade dessa substância se modifica com a variação da temperatura conforme a tabela a seguir. 4630 3220 água)de(g/100gdeSolubilidaC)(ºaTemperatur Se a solução for resfriada para 20 ºC, a massa, em gramas, do sal que irá precipitar será igual a a) 48,0 b) 28,0 c) 22,4 d) 13,8 8. (PUCCamp-SP) Evapora-se totalmente o solvente de 250 mL de uma solução aquosa de cloreto de magnésio de concentração 8,0g/L. Quantos gramas de soluto são obtidos? 9. Um estudante analisou três soluções aquosas de cloreto de sódio, adicionando 0,5 g deste mesmo sal em cada uma delas. Após deixar as soluções em repouso em recipientes fechados, ele observou a eventual presença de precipitado e filtrou as soluções, obtendo as massas de precipitado mostradas no quadro abaixo. O estudante concluiu que as soluções originais 1, 2 e 3 eram, respectivamente, a) não saturada, não saturada e saturada. b) não saturada, saturada e supersaturada. c) saturada, não saturada e saturada. d) saturada, saturada e supersaturada. e) supersaturada, supersaturada e saturada. 10. São dissolvidos 200g de cloreto de sódio em água suficiente para 2 litros de solução. Qual é a concentração comum dessa solução? 11. Abaixo é mostrado um gráfico de solubilidade de diferentes substâncias em água. Observando atentamente o gráfico, assinale a opção que apresenta a afirmativa INCORRETA. a) O nitrito de sódio é o mais solúvel a 0 ºC. b) A solubilidade do NaCℓ varia pouco com o aumento da temperatura. c) Em torno de 37 ºC o cloreto de potássio e clorato de potássio possuem a mesma solubilidade. d) Adicionando-se 100 g de clorato de potássio à 100 mL de água a 100 ºC restarão cerca de 50 g do sal sem se dissolver. e) Adicionando-se 100 g de cloreto de cálcio à 100 mL de água a 10 ºC restarão cerca de 70 g do sal sem se dissolver. 12. A concentração comum de uma solução é de 20g/L. Determine o volume, em mL, dessa solução, sabendo que ela contém 75g de soluto. 13. No gráfico abaixo, apresentamos a curva de solubilidade do nitrato de potássio, KNO3, em função da variação da temperatura, expressa em gramas de solubilidade do KNO3, por 100 g de água. Em relação ao gráfico, foram feitas as seguintes afirmações: I. Ao dissolvermos 60 g deste sal em água a 25 ºC, teremos uma solução insaturada. II. Ao resfriarmos a solução saturada de 70 ºC a 40 ºC, ocorrerá a precipitação de 30 g do sal. III. Ao aquecermos a solução saturada de 10 ºC a 40 ºC, a massa do sal presente na solução será de 30 g. IV. Ao dissolvermos 10 g deste sal em água a 25 ºC, teremos uma solução supersaturada. V. Ao resfriarmos uma solução saturada de 70 ºC a 40 ºC, a massa do sal que permanece dissolvido na solução será de 60 g. São corretas as afirmações: a) I apenas. b) V apenas. c) I, V e IV. d) II e III apenas. e) I, II, III e IV. Sobre o autor: Claudinei O. Oliveira, professor de Química e autor do blog QuÍmIcA a FaVoR dA vIdA, disponível em www.quimicafv.blogspot.com
