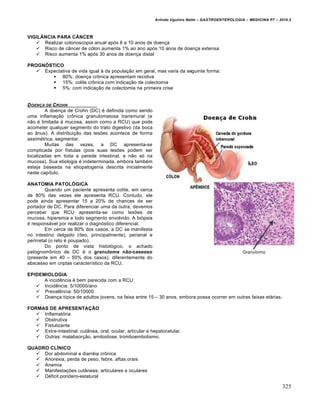
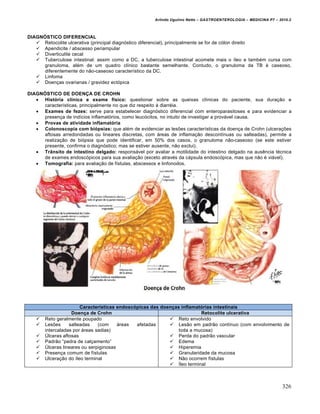
Este documento resume informações sobre a doença por refluxo gastroesofágico (DRGE). Apresenta definições, fatores de risco, mecanismos fisiopatológicos e manifestações clínicas da DRGE. Discute a epidemiologia, fatores de defesa e agressão da mucosa esofágica, e sintomas típicos e atípicos da condição.

















































![Arlindo Ugulino Netto – GASTROENTEROLOGIA – MEDICINA P7 – 2010.2
274
Hepatite Auto-imune: dosagem fenotípica, avaliando a presença de genes, FAN, anti-ML e anti-LKM
Cirrose Biliar primária: anti-mitocondrial
Doenças Metabólicas:
Hemocromatose: ferro, ferritina, TIBC
Doença de Wilson: cobre e ceruloplasmina
Deficiência de alfa-1-antitripsina: alfa-1-antitripsina sérica. Geralmente esses pacientes apresentam mais
manifestações pulmonares que hepáticas.
A avaliação laboratorial desses pacientes é importante para estabelecer a pontuação de acordo com a escala de
CHILD-PUGH e MELD/PELD. Através delas, estabelecer a classificação das doenças de acordo com sua gravidade.
Assim temos:
Child-Pugh.
O escore de Child-Pugh é calculado somando os pontos dos cinco fatores, e varia de 5 a 15. A classe de Child-Pugh é A
(escore de 5 a 6 ), B (7 a 9), ou C (acima de 10). Em geral, o critério de inclusão para cadastro em filas de transplante hepático é a
classificação do paciente como Grau B. Se o paciente apresentar Grau A ou C, não apresenta prioridade no transplante.
Meld/Peld.
O modelo matemático MELD utiliza três parâmetros laboratoriais por meio dos quais se obtêm facilmente nos exames de
rotina de qualquer hepatopatia crônica. A equação para calcular o escore MELD = {9,57 x loge creatinina mg/dL + 3,78 x loge bilirrubina
(total) mg/dL + 11,20 x loge INR + 6,42], por meio da qual podemos chegar a um resultado aproximadamente inteiro. O valor máximo
de creatinina vai até 4.
Para conceituação de hepatopatia grave, aceita-se atualmente o valor do MELD igual ou maior que 15. Estes pacientes são
indicados para a realização de transplante hepático. Entretanto abaixo desse valor, permanecem fora da lista de transplante.
EXAMES ENDOSCÓPICOS E DE IMAGEM
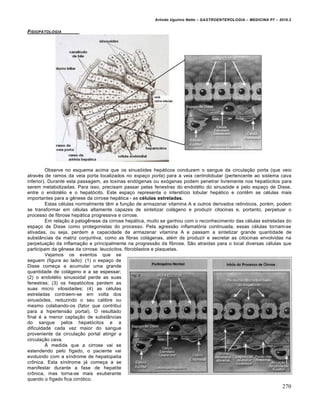
Do ponto de vista endoscópico, podemos observar a presença das varizes esofágicas, varizes gástricas e
colônicas. Além disso, a endoscopia permite observar sinais da chamada gastropatia hipertensiva, quando a mucosa
gástrica se mostra semelhante a couro de cobra.
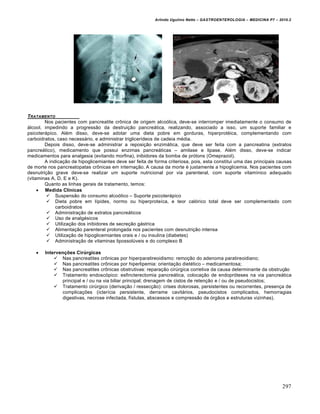
O papel dos exames radiológicos na avaliação da cirrose hepática inclui (1) a caracterização das manifestações
morfológicas da doença; (2) avaliação da vascularização hepática e extra-hepática; (3) detectar e estimar os efeitos da
hipertensão portal; e (4) identificar tumores hepáticos, diferenciando o carcinoma hepatocelular (HCC) de outros tipos de
tumor. Entre os exames mais solicitados temos: ultrasonografia (Doppler para avaliar o fluxo da veia porta), tomografia
computadorizada, ressonância magnética, cintilografia hepática.
As alterações mais comumente visualizadas de acordo com o grau
evolutivo da doença são:
Nodularidade da superfície hepática.
Heterogeneidade do parênquima hepático.
Alargamento da porta hepatis e da fissura interlobar.
Redução volumétrica do lobo hepático direito e do segmento médio do
lobo hepático esquerdo.
Aumento volumétrico do lobo caudado e do segmento lateral do lobo
hepático esquerdo.
Identificação de nódulos regenerativos. Neste caso, a RM constitui método
superior aos demais.](https://image.slidesharecdn.com/gastroenterologia-completa-170904035048/85/Gastroenterologia-completa-66-320.jpg)