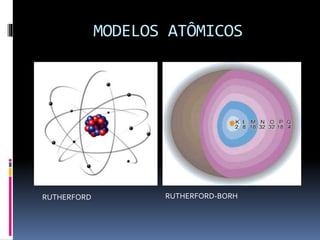
O documento discute os conceitos fundamentais de eletroquímica, incluindo que eletroquímica envolve transformações químicas mediadas por elétrons ou energia elétrica, processos de oxirredução como a ferrugem e a oxidação de maçãs, e o cálculo do número de oxidação de íons e compostos.