1) O documento descreve o conceito, definição, patogênese, quadro clínico e conduta diagnóstica e terapêutica do choque.
2) O choque é caracterizado por perfusão tissular reduzida que pode levar a disfunção orgânica grave e morte se não tratado.
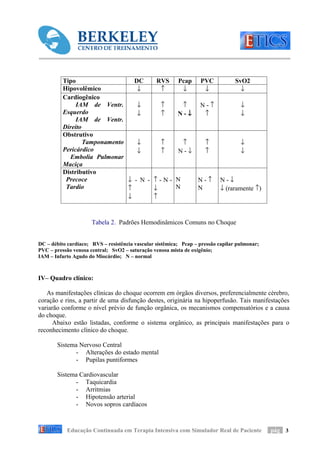
3) Existem quatro tipos de choque baseados na causa: hipovolêmico, obstrutivo, cardiogênico e distributivo.



![8. Proceder monitorizações invasivas de pressão arterial média (PAM), pressão venosa
central (PVC) e, uso do cateter de Swan-Ganz para avaliação da performance de
ventrículos esquerdo e direito, e débito cardíaco.
9. Solicitar exames complementares: hemograma completo, gasometria arterial, lactato
sérico, glicose, uréia, creatinina, eletrólitos, coagulograma, ECG, radiografia de tórax,
EAS e, culturas dos materiais orgânicos relevantes quando da suspeita de Sepse.
10. Neste último caso, iniciar cobertura antibiótica empírica, enquanto exames mais
específicos são avaliados.
11. Se há suspeita de Insuficiência Suprarrenal – refratariedade à reposição volêmica e
drogas vasopressoras – fazer Dexametasona EV ( não alterará o teste de estimulação
da Cortrosina [ACTH]).
12. Se houver evento isquêmico cardiogênico, avaliar uso de trombólise ou cateterização
cardíaca de emergência.
Droga Efeito Predominante Efeito Predominante Dose Uso Clínico
Cardíaco Periférico
Dobutamina + Freqüência cardíaca (β1) + Dilatação arterial (β2) 1 – 10 µg/kg/min Choq.
+++ Contratilidade (β1, α) Cardiogênico,
séptico e obstrutivo
Dopamina ++ Freqüência cardíaca ++ Constric. arterial (α) 1 – 15 µg/kg/min Todas as formas de
(β1) +++ Dilatação arterial renal, ( dose renal 1 – 4 choque
++ Contratilidade (β1, α) mesentérica, cerebral e µg/kg/min)
coronária (DA1 e DA2)
Adrenalina +++ Freqüência cardíaca ++ Constric. arterial (α) 1 – 10 µg/kg/min Anafilaxia e choque
(β1) refratário
+++ Contratilidade (β1, α)
Noradrenalina ++ Freqüência cardíaca +++ Constric. arterial (α) 2 – 20 µg/kg/min Choque séptico e
(β1) refratário
++ Contratilidade (β1, α)
Nitroprussiato Sem efeito direto +++ Dilatação arterial 0.5 - 8µg/kg Choq.
++ Venodilatação /min Cardiogênico,
séptico e obstrutivo
Nitroglicerina Sem efeito direto +++ Venodilatação 5 – 66 µg/min Choq.
+ Dilatação arterial Cardiogênico,
séptico e obstrutivo
Tabela 3. Agentes farmacológicos comumente usados em pacientes com Choque
Educação Continuada em Terapia Intensiva com Simulador Real de Paciente pág 5](https://image.slidesharecdn.com/choque-130212172644-phpapp02/85/Choque-5-320.jpg)




