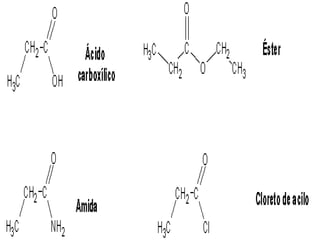
O documento classifica e descreve as propriedades dos ácidos carboxílicos. São divididos em monocarboxílicos e dicarboxílicos. São ácidos fracos e podem formar ligações de hidrogênio. Suas propriedades como ponto de ebulição dependem do tamanho da cadeia carbônica. Reagem com bases formando sais e podem reagir para formar ésteres ou ligações peptídicas.