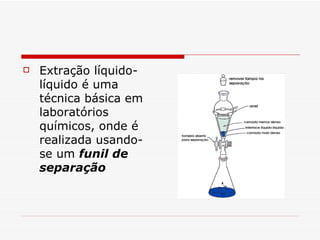
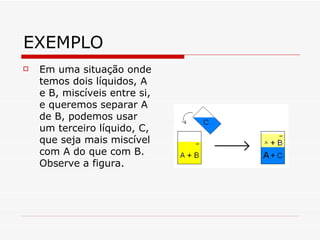
A extração líquido-líquido é um método para separar compostos com base em sua solubilidade em dois líquidos imiscíveis, geralmente água e um solvente orgânico. O processo envolve agitar as fases líquidas em um funil de separação para que os compostos se distribuam entre elas com base em sua solubilidade relativa. A técnica é amplamente utilizada em laboratórios químicos e no preparo de café.