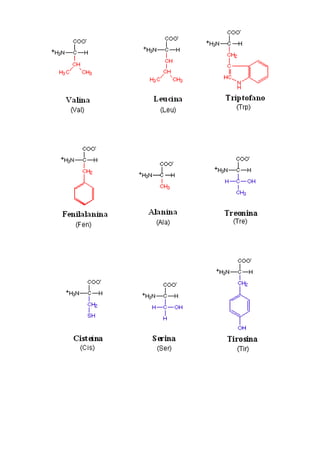
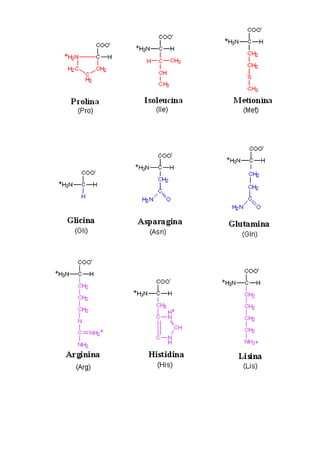
O documento resume as principais características dos aminoácidos, incluindo sua estrutura química básica, os 20 aminoácidos essenciais para o corpo humano, as classificações de acordo com o tipo de radical e propriedades químicas como ionização e estereoisomeria.