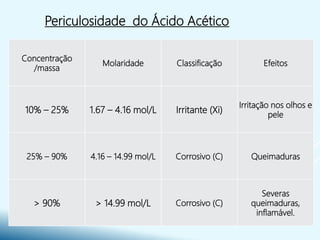
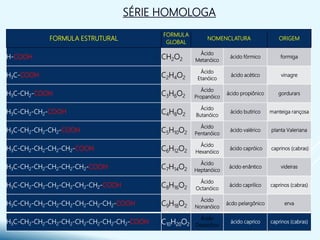
- O documento discute os ácidos carboxílicos, incluindo sua classificação, estrutura, nomenclatura e série homóloga.
- São classificados de acordo com o número de grupos carboxila presentes e tipo de cadeia.
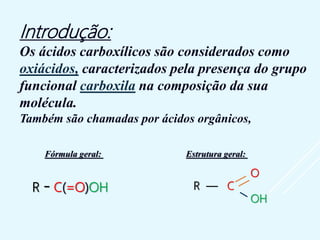
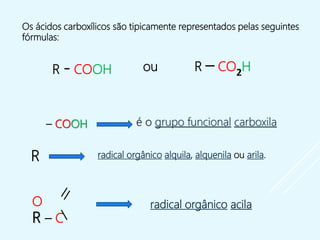
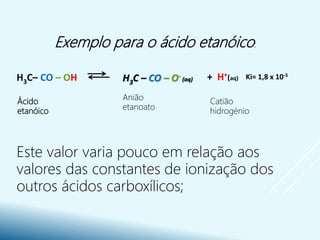
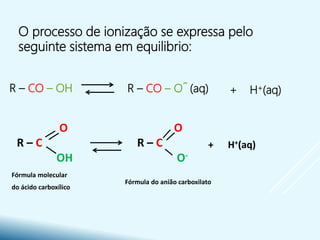
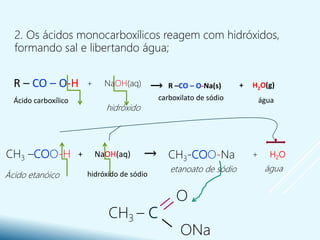
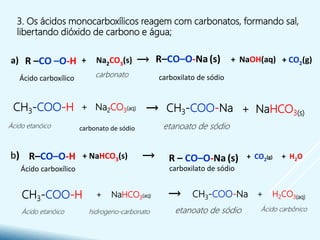
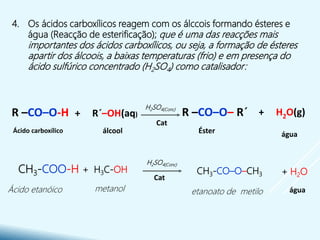
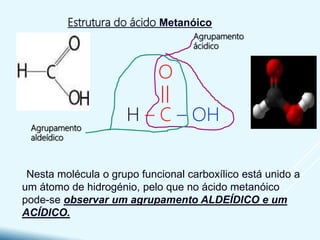
- São caracterizados pela presença do grupo funcional carboxila -COOH e formam sais e ésteres em reações químicas.
















![MÉTODOS DE OBTENÇÃO DE ÁCIDOS CARBOXÍLICOS
1. Por oxidação de álcoois e aldeídos
O álcoois primários e os aldeídos podem ser oxidados
utilizando permanganatos, para produzir ácidos
carboxílicos:
1ª etapa:
2ª etapa:
+ H2OR - CHO[O]R - CH2OH
AldeídoÁlcool
R - COOHR - CHO
ácido carboxílicoAldeído
[O]
Oxidação
Oxidação](https://image.slidesharecdn.com/014estudodoscidosdicarboxilicos-151103080145-lva1-app6891/85/Estudo-dos-acidos-dicarboxilicos-013-27-320.jpg)
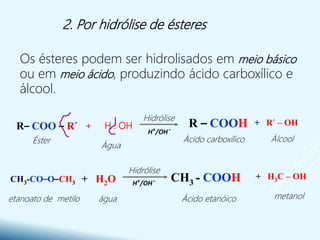







![ Em solução aquosa o ácido etanóico separa-se em iões:
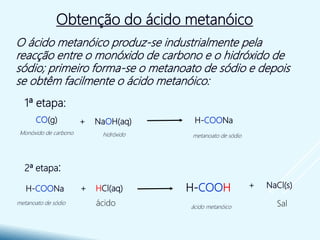
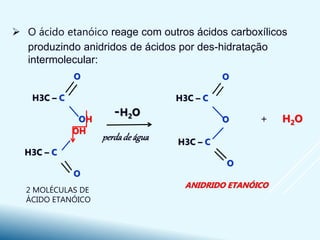
O ácido etanóico reage com os metais que se encontram primeiro
que o Hidrogénio na série de actividade dos metais, formando um sal
e libertando hidrogénio:
+ H3O+(aq)H3C–COO-(aq)H3C – COOH + H2O
anião acetato catião hidrónioÁcido carboxílico
+ H2(g)[H3C – COO
-]2 Mg (s)+ Mg(s)2H3C–COOH
etanoato de Magnésio
Ácido etanóico Magnésio](https://image.slidesharecdn.com/014estudodoscidosdicarboxilicos-151103080145-lva1-app6891/85/Estudo-dos-acidos-dicarboxilicos-013-39-320.jpg)


![CH3 - CHO
Oxidação
[ O ]
b) Oxidação do acetaldeído
o ácido acético é fabricado a partir do
acetaldeido(etanal), por oxidação e em
presença de catalisadores:
CH3-COOH
acido acético](https://image.slidesharecdn.com/014estudodoscidosdicarboxilicos-151103080145-lva1-app6891/85/Estudo-dos-acidos-dicarboxilicos-013-43-320.jpg)