O documento discute o conceito de pH e como calcular o pH de soluções aquosas. Explica que o pH é definido como -log[H3O+] e relaciona o pH com a concentração de íons hidrogênio. Também aborda como o valor de Kw, a constante de autoionização da água, varia com a temperatura e como isso afeta o pH.

![A escala de Sorensen permite traduzir a concentração de iões H+ através da
relação:
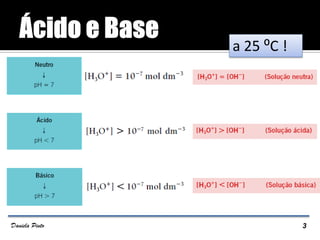
A 25 ºC, para a água pura obtemos:
2Daniela Pinto
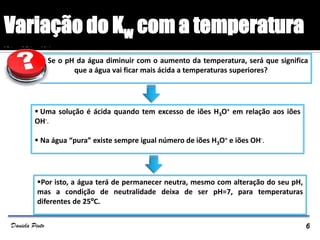
Qual será o valor do
pH da água a 25º C?
Como [H3O+] = 110-7 mol dm-3
pH = - log (110-7) pH = 7
𝑝𝐻 = −𝑙𝑜𝑔 𝐻3 𝑂+ ⇔ 𝐻3 𝑂+ = 10−𝑝𝐻](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-2-320.jpg)
![O conceito de pH
Podemos também definir pOH:
pOH = - log [OH-]
Relação entre pH e pOH
pH + pOH = pKw
pKw = - log Kw
À temperatura de 25⁰C:
pH + pOH = 14
EXERCÍCIOS
Determine o valor de pH de cada uma das
seguintes soluções (a 25ºC), cuja
concentração de iões hidrónio é:
i. 110-7 mol dm-3
ii. 110-6 mol dm-3
iii. 510-6 mol dm-3
iv. 110-5mol dm-3
v. 2,310-4 mol dm-3
4Daniela Pinto](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-4-320.jpg)

![FORÇA DOS ÁCIDOS E DAS BASES
Se a solução for a de um ácido monoprótico forte, a concentração de H3O+ na
solução é aproximadamente igual à do ácido porque a reação de ionização é
praticamente completa, e o grau de ionização aproximadamente igual a 1.
Para efetuar o cálculo do pH de uma solução é preciso conhecer a concentração de
H3O+.
)(3)(2)( )( aqaqaq OHCllOHHCl
EXERCÍCIOS
Determine o pH de uma solução de ácido clorídrico, HCl, 0,15 mol dm-3.
Como o ácido é forte, ioniza-se completamente, logo [HCl]=[H3O+] 0,15 mol dm-3.
Então como pH = -log [H3O+] pH = -log (0,15) = 0,82
R:
7Daniela Pinto](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-7-320.jpg)
![EXERCÍCIOS
R: A reação de ionização é traduzida pela equação seguinte:
HNO3 (aq) + H2O (l) NO3
- (aq) +H3O+ (aq)
Como a ionização é completa, o grau de ionização igual a 1, [H3O+]final = [HNO3]inicial,
pelo que [H3O+]final = 5,0 x 10-2 mol dm-3, o que implica que pH = -log 5,0 x 10-2, isto
é, pH = 1,3.
Determine, a 25 ºC, o pH de uma solução aquosa de ácido nítrico, HNO3, 5,0 x 10-2 mol dm-3
Notas:
• Para soluções aquosas de bases fortes, como NaOH e KOH, hidróxido de sódio e
hidróxido de potássio, respetivamente, a determinação da concentração de OH- é
efetuada de um modo semelhante à determinação da concentração de H3O+ para
ácidos fortes.
• Para soluções aquosas de ácidos ou bases fracas, a concentração de H3O+ e/ou OH-
vai depender da constante de equilíbrio da reação em causa, uma vez que estas
reações de ionização não são completas.](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-9-320.jpg)
![A reação de ionização é traduzida pela equação seguinte:
CH3COOH (aq) + H2O (l) H3O+ (aq) + CH3COO- (aq)
Quando se atinge o equilíbrio, para o mesmo volume, os valores das concentrações
das espécies químicas são:
[CH3COOH]equilíbrio = 5,0 x 10-2 – x ; [CH3COO-]equilíbrio = x ; [H3O+] = x
A partir do valor de Ka do ácido, à temperatura referida, pode determinar-se o valor
de x e a partir deste o pH da solução.
Determine, a 25 ºC, o pH de uma solução aquosa de ácido acético,
CH3COOH, 5,0 x 10-2 mol dm-3.
EXERCÍCIOS
R:](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-10-320.jpg)
![A reação de ionização é traduzida pela equação seguinte:
HCl (aq) + H2O (l) Cl- (aq) + H3O+ (aq)
O grau de ionização ser 1, significa que o ácido está completamente ionizado,
logo
[HCl ] = [H3O+] = 0,1 mol dm-3 ; [HCl ]= 0 mol dm-3 e como [H3O+] [OH- ]= 1 10-14
[OH- ] = 1 10-13 mol dm-3
O ácido clorídrico é um ácido forte ( 1).
Quais as concentrações de H3O+, OH- e 0,1 mol dm-3 a 25ºC?
EXERCÍCIOS
R:](https://image.slidesharecdn.com/6-oph-140509033200-phpapp02/85/6-o-p-h-11-320.jpg)