[1] O documento apresenta os conceitos fundamentais da Teoria Cinética dos Gases, incluindo as leis de Boyle, Charles e Gay-Lussac;
[2] A teoria explica o comportamento dos gases com base no movimento aleatório das partículas que os compõem, e como variáveis como pressão, volume e temperatura influenciam esse movimento;
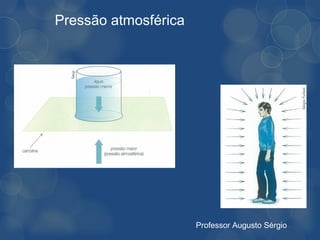
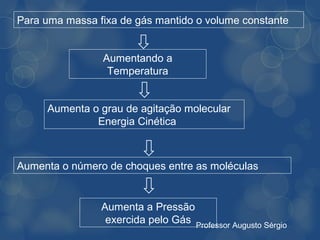
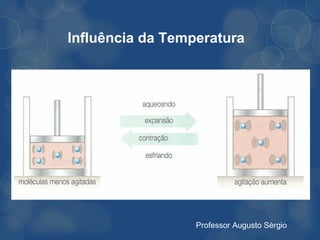
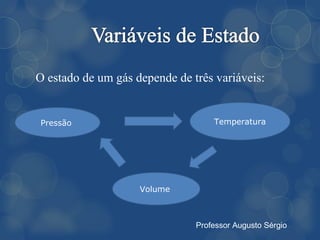
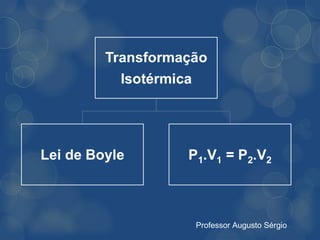
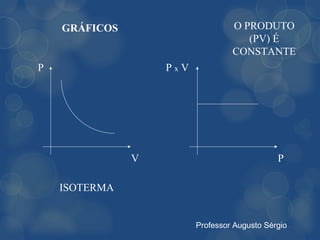
[3] A lei de Boyle estabelece que, em temperatura constante, o volume de um gás varia inversamente à pressão aplicada.