substituicao nucleofilica aromatico .pdf
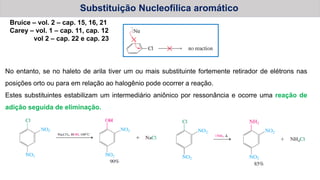
- 1. Substituição Nucleofílica aromático Bruice – vol. 2 – cap. 15, 16, 21 Carey – vol. 1 – cap. 11, cap. 12 vol 2 – cap. 22 e cap. 23 No entanto, se no haleto de arila tiver um ou mais substituinte fortemente retirador de elétrons nas posições orto ou para em relação ao halogênio pode ocorrer a reação. Estes substituintes estabilizam um intermediário aniônico por ressonância e ocorre uma reação de adição seguida de eliminação.
- 2. Substituição Nucleofilica aromático Carga negativa está fortemente estabilizada 1ª Etapa – adição nucleofílica 2ª Etapa – eliminação
- 3. Substituição Nucleofilica aromático Uma variedade de substituintes podem ser adicionado sendo que o grupo nucleofílico (base) deve ser mais forte que o grupo de saída.
- 4. Substituição Nucleofilica aromático Reatividade do Grupo de saída Porque está reatividade??? Efeito indutivo
- 5. Substituição Nucleofílica aromático Quando uma base forte, tal como o NH2 - reage com o haleto de arila – eliminação/adição Clorobenzeno-1-14C benzenamina-1-14C benzenamina-2-14C Neste caso o anel não precisa possuir um grupo retirador de elétrons e o substituinte nem sempre se ligal ao carbono que continha o grupo de saída. Mas então o que está acontecendo???
- 6. Substituição Nucleofílica aromático O mecanismo proposto envolve um intermediário benzino – reação eliminação/adição 1º Etapa – Eliminação do próton da posição orto ao grupo de saída sp2 – orbital hibridizado está perpendicular ao sistema do aromático Anel altamente tensionado 2º Etapa – Adição ocorre em ambos carbonos tensionados
- 8. Os fenóis também podem ser obtidos a partir de sais de arenodiazônio. Substituição Nucleofílica aromático Este caso envolve a decomposição do sal de diazônio formando o carbocátion instável (íon arênio) Portanto, se a diazotização for feita a baixas temperaturas (pouco acima de 0 °C - 5 °C), o sal de diazônio é estável e pode reagir com vários nucleófilos. Se a solução aquosa é aquecida, a água atua novamente como o nucleófilo e um fenol é formado A partir da amina. O aril cátion é um intermediário e esta é uma reação SN1 em um aromático anel.
- 9. Substituição Nucleofílica aromático Síntese de haletos de arila a partir do sal de diazônio – reações de Sandmeyer
- 11. Heterociclos Aromáticos Pirrol e Imidazol sofrem reações de substituição eletrofílica no aromático Porque a posição C2 é predominante? A substituição eletrofílica aromática ocorre principalmente em C2, porque o intermediário durante o ataque em C2 tem uma maior estabilizaçõ por ressonância.
- 12. Heterociclos Aromáticos Estruturas dos intermediários que podem ser formados a partir da reação de um eletrófilo nas posições C2 e C3. Reatividade dos heterociclos Porque está ordem de reatividade???
- 14. Piridina e pirimidina sofrem reações de substituição eletrofílica no aromático Heterociclos Aromáticos Porque a posição C3 é predominante? lenta rápida
- 15. Heterociclos Aromáticos Piridina - Porque a posição C3 é predominante? Menos estável Menos estável
- 16. Heterociclos Aromáticos Reatividade frente a substituição eletrofílica aromática
- 17. Heterociclos Aromáticos Substituição nucleofílica aromática A piridina sofre substituição nucleofilica aromática nos carbono C2 e C4 Mais estável Mais estável
- 18. Heterociclos Aromáticos Se os grupos de saída no C-2 e no C-4 são diferentes, o nucleófilo que se aproxima substituirá preferencialmente a base mais fraca.
- 19. Exercícios 1. Como você pode formar os seguintes compostos a partir do composto correspondente. 2. Proponha um mecanismo para a seguinte reação.
- 20. Exercícios 3. Explique a regiosseletividade observada na seguinte reação. 4. Dê o produto que pode ser obtido na reação dos seguintes compostos com amideto de sódio em amônia liquida.
- 21. Exercícios 5. Explique porque a piridina sofre substituição somente nos carbonos C-2 e C-4. 6. Como você poderia converter os compostos aromáticos nesses derivados.
- 22. Exercícios 7. Propor uma síntese eficiente para cada uma das seguintes transformações.
- 23. 8. Dê o produto das seguintes reações. Exercícios