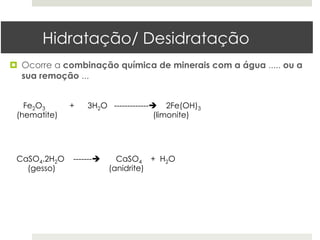
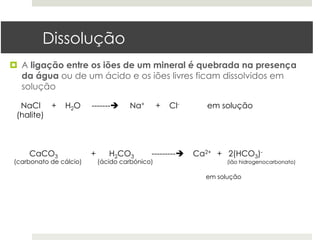
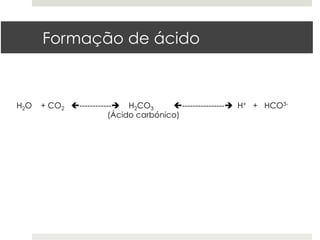
A meteorização química ocorre através de processos como hidratação/desidratação, dissolução, formação de ácido, hidrólise, oxidação/redução. Estes processos quebram as ligações entre iões dos minerais ou alteram seu estado de oxidação, levando à formação de novos minerais ou à desintegração do mineral original. A humidade e a temperatura afetam as taxas destas reações químicas.