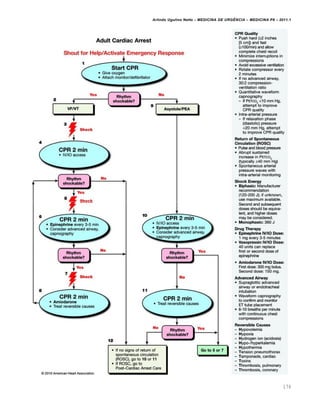
[1] O documento discute o protocolo de atendimento ao politraumatizado segundo o Advanced Trauma Life Support (ATLS), incluindo a avaliação inicial, preparação, triagem e abordagem sistemática dos pacientes.
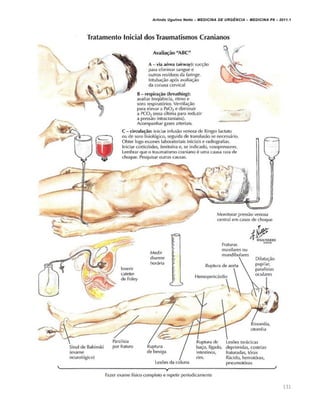
[2] O objetivo do ATLS é realizar uma avaliação rápida para identificar e tratar imediatamente ameaças à vida, priorizando as lesões que colocam o paciente em maior risco.
[3] A triagem classifica os pacientes de acordo com suas necessidades para que os casos mais graves sejam atendidos primeiro de

















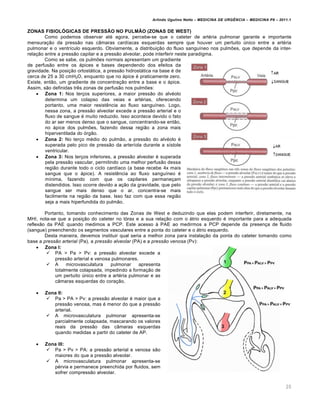


























































![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
89
Portanto, segundo esta classifica†…o, toda subst‡ncia capaz de doar um •on H
+
‚ classificada como um ƒcido;
toda subst‡ncia capaz de receber este •on H
+
‚ classificada como base. A depender da capacidade em doar estes •ons
ou de receb€-los, classificados estas subst‡ncias como fortes ou fracas.
medida que um ƒcido se torna mais forte, a sua base conjugada torna-se mais fraca ou ƒ medida que as bases
tornam-se mais fortes, os seus ƒcidos conjugados tornam-se mais fracos. De forma geral, quando ocorre uma rea†…o
ƒcido-base de Br¡nsted-Lowry, a posi†…o de equil•brio situa-se na dire†…o dos ƒcidos e bases mais fracos.
DEFINIÇÃO DE pH
“pH” ‚ o s•mbolo para a grandeza f•sico-qu•mica potencial hidrogeni•nico. Essa grandeza indica a acidez,
neutralidade ou alcalinidade de uma solu†…o aquosa. Em outras palavras, o pH refere-se a uma medida que indica se
uma solu†…o l•quida ‚ ƒcida (pH < 7, a 25 ˜C), neutra (pH = 7, a 25 ˜C), ou bƒsica/alcalina (pH > 7, a 25˜C). Uma
solu†…o neutra s„ tem o valor de pH = 7 a 25 ˜C, o que implica varia†ˆes do valor medido conforme a temperatura.
Matematicamente, o "pH" equivale ao sim‚trico do logaritmo (cologaritmo) de base 10 da atividade dos •ons a
que se refere.
Para •ons H
+
: pH = -log10[aH
+
], sendo que aH
+
representa a atividade
Em solu†ˆes dilu•das (abaixo de 0,1 mol dm
−3
), os valores da atividade se aproximam dos valores da
concentra†…o, permitindo que a equa†…o anterior seja assim escrita: pH = -log10[H
+
]
Tomaremos como base do nosso estudo a mol‚cula da ƒgua, considerada uma subst‡ncia neutra. Levando-se
em considera†…o que a mol‚cula de ƒgua se dissolve muito mal, temos:
H2O H
+
+ OH
-
A dissocia†…o da ƒgua forma 1 mol‚cula dissociada (formando
um pr„ton H
+
) para cada 10.000.000 mol‚culas n…o dissociadas.
Desta forma, a concentra†…o de H
+
na ƒgua ‚ de:
1/10.000.000 ou 0,0000001 ou 1/10
7
ou 1x10
-7
ou 1nEq/l
Portanto, a concentra†…o de hidrog€nio em uma solu†…o
que s„ cont‚m ƒgua ‚ de 0,0000001 ou 1x10
-7
.
Entretanto, ‚ dif•cil para a nossa mente imaginar um
n‰mero t…o pequeno como ‚ a rela†…o de dissocia†…o dos
pr„tons de ƒgua. Por isso, o pH foi criado. O pH nada mais ‚ que
uma fun†…o logar•timica inversa (negativa) da concentra†…o de
hidrog€nio. Sua utiliza†…o serve para facilitar a compreens…o e
compara†…o destes n‰meros muito pequenos, utilizando-se o
logaritmo negativo da concentra†…o de H
+
.
Desta forma, jogando-se o valor de dissocia†…o da ƒgua
na fun†…o logar•tmica do pH, teremos: pHH2o =-log1010
-7
= 7.
Portanto, sendo a ƒgua uma subst‡ncia neutra, o pH=7
(que representa uma concentra†…o de •ons hidrog€nio de 1x10
-7
dissolvidos em ƒgua), para a qu•mica, representa um ponto
neutro na escala de pH. Todavia, para a bioqu•mica, este valor
pode ser aumentado a um intervalo (7,35 – 7,45), como veremos
mais adiante.
SISTEMAS TAMPÃO E EQUILÍBRIO ÁCIDO-BÁSICO
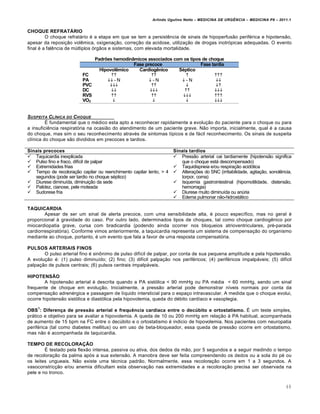
A concentração de hidrogênio no plasma ‚ determinada pela rela†…o entre o di„xido de carbono (CO2) e o
bicarbonato (HCO3
-
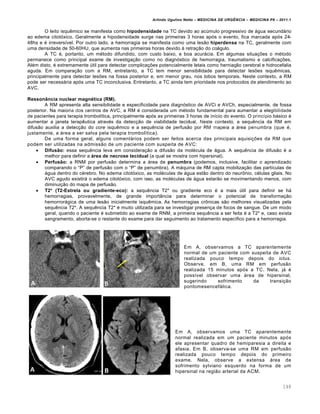
), nesta ordem. Esta rela†…o ‚ expressa pela equação de Henderson, sendo ela:
[H
+
]sangue = 24 x pCO2 / HCO3
-
pH = 7,4 representa uma concentra†…o de H
+
de 40 nanomol/L
pH = 7,1 representa uma concentra†…o de H
+
de 80 nanomol/L
Portanto, utilizando-se esta f„rmula, toda vez que tivermos um aumento da press…o parcial de CO2 (pCO2 ou
PaCO2), observamos um aumento das concentra†ˆes de H
+
; toda vez que tivermos um aumento do HCO3
-
, observamos
uma diminui†…o dos •ons H
+
. Portanto, a concentra†…o de hidrog€nio ‚ diretamente proporcional Œ pCO2 e indiretamente
proporcional Œs concentra†ˆes de bicarbonato.](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-89-320.jpg)




![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
94
ACIDOSE OU ACIDEMIA METAB’LICA: ↓HCO3
-
, ↓pH, ↓pCO2
A diminui†…o do bicarbonato (HCO3
-
) causa um maior consumo de CO2 para a maior produ†…o de ƒcido
carb•nico e, deste modo, uma maior produ†…o de H
+
, o que diminui o pH. Esta condi†…o causa uma hiperpneia no intuito
de diminuir a pCO2 e tentar compensar este excesso de ƒcido metab„lico.
Portanto, a diminui†…o de HCO3
-
, associada a uma resposta secundƒria que diminua a pCO2, justifica a acidose
metab„lica.
As seguintes condi†ˆes podem causar acidose metab„lica;
Aumento da produ†…o de ƒcidos metab„licos:
acidose lƒtica, cetoacidose diab‚tica.
Adi†…o de ƒcidos metab„licos ao corpo por
ingest…o, ou infus…o
Excre†…o prejudicada de ƒcidos: insufici€ncia
renal.
Perda de bicarbonato: diarreia (como ocorre na
c„lera), f•stulas enterocut‡neas, tubulopatias.
Choques s‚pticos e hipovol€micos (devido Œ
acidose causada pela anaerobiose difusa).
Perda de bases dos l•quidos corporais:
Acidose tubular renal: defeito na excre†…o
renal de H
+
ou na reabsor†…o de HCO3
-
, ou
de ambos
Diarr‚ia: perda de grande quantidade de
bicarbonato nas fezes
V•mitos do conte‰do intestinal
Diabete mellito: aumento da produ†…o de
ƒcidos metab„licos (ƒcido acetoac‚tico)
Ingest…o de ƒcido (AAS, ƒlcool met•lico)
Insufici€ncia renal: filtra†…o glomerular
excre†…o de fosfatos e NH4
+
reabsor†…o
de bicarbonato.
ALCALOSE OU ALCALEMIA METAB’LICA: ↑HCO3
-
, ↑pCO2, ↑pH
O aumento do bicarbonato causa um maior consumo de H
+
para maior produ†…o de CO2 (o que aumenta o
pCO2). O consumo de H
+
aumenta o pH sangu•neo.
Portanto, o aumento de HCO3
-
, associado a uma resposta secundƒria que aumente a pCO2, justifica a alcalose
metab„lica.
Assim como a alcalose respirat„ria, a alcalose metab„lica ‚ uma condi†…o rara, geralmente causada por
medicamentos, e n…o por condi†ˆes org‡nicas. As principais situa†ˆes que cursam com este quadro s…o:
Perda de ƒcidos fixos: v•mitos de conte‰do
gƒstrico (como ocorre por estenose pil„rica).
Ingest…o de ƒlcalis (soda cƒustica).
Alcalose de contra†…o que ocorre na desidrata†…o.
Excesso de aldosterona: reabsor†…o de s„dio +
secre†…o de H
+
+ reabsor†…o de HCO3
-
+ [K
+
]
Administra†…o de diur‚ticos (exceto os inibidores
da anidrase carb•nica): FG Fluxo tubular
reabsor†…o de s„dio e excre†…o de potƒssio +
secre†…o de H
+
+ reabsor†…o de HCO3
-
.
ALTERA‚ƒES ESPERADAS NOS DISTŽRBIOS …CIDO-B…SICOS
Como vimos anteriormente, diante de altera†ˆes do pH decorrente de um dist‰rbio pulmonar ou renal, o
organismo lan†a m…o de uma resposta secundƒria que realiza o evento contrƒrio, no intuito de atenuar o desequil•brio.
Por meio de f„rmulas matemƒticas, podemos determinar a eficƒcia da resposta secundƒria:
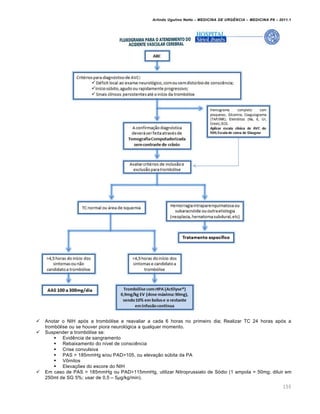
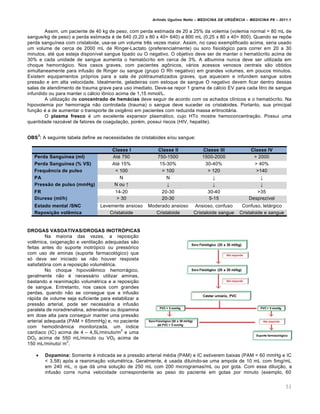
Tabela de Compensa‚ƒo †cido-B‡sico
Dist•rbio prim‡rio Altera‚„es esperadas
Acidose metab„lica pCO2 = 1,5 x HCO3 + (8 £ 2)
Alcalose metab„lica pCO2 = 0,7 x HCO3 + (21 £ 2)
Acidose respirat„ria aguda pH = 7,4 – [0,008 x (pCO2 – 40)]
Acidose respirat„ria cr•nica pH = 7,4 – [0,003 x (pCO2 – 40)]
Alcalose respirat„ria aguda pH = 7,4 + [0,008 x (40 – pCO2)]
Alcalose respirat„ria cr•nica pH = 7,4 + [0,017 x (40 – pCO2)]
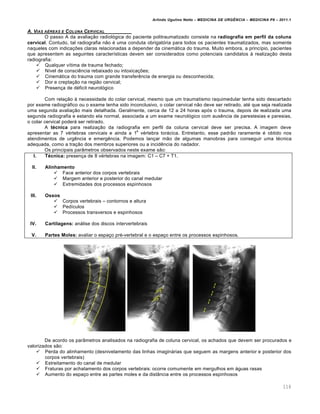
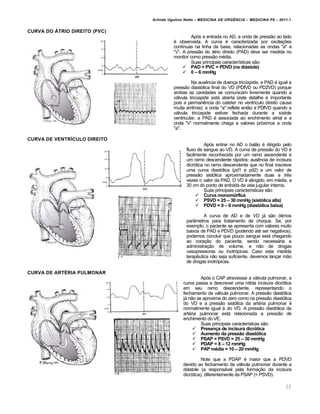
Veremos mais adiante os valores gasom‚tricos normais para todas essas variƒveis. Entretanto, jƒ
exemplificando o efeito ben‚fico da compensa†…o respirat„ria sobre o pH, observemos o seguinte quadro (os valores de
pH foram calculados a partir da equa†…o de Henderson-Hasselbach):
Status ‡cido-b‡sico HCO3
-
pCO2 pH Coment‡rios
Normal 24 40 7,40 A
Acidose metab„lica 9 22 7,23 B
Ac. Met. + Ac. Resp. 9 40 6,98 C
Ac. Met. + Alc. Resp. 9 15 7,40 D](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-94-320.jpg)



![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
98
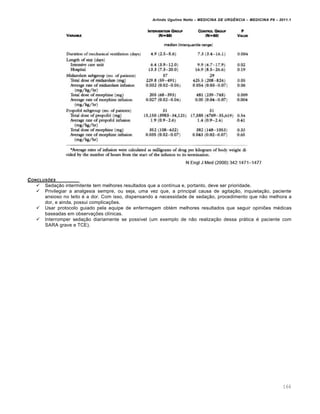
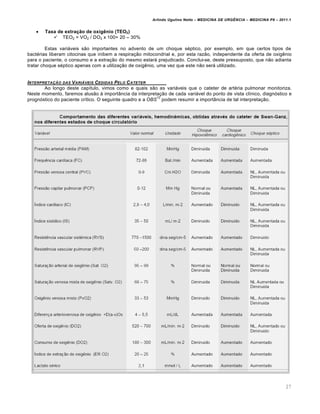
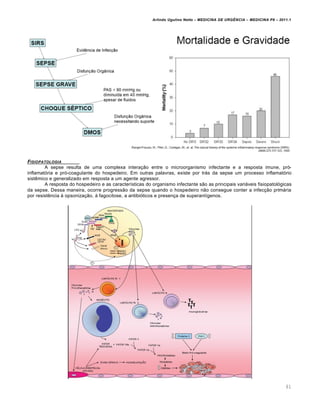
Tabela de Compensação Ácido-Básico
Distúrbio primário Alterações esperadas
Acidose metab„lica pCO2 = 1,5 x HCO3 + (8 £ 2)
Alcalose metab„lica pCO2 = 0,7 x HCO3 + (21 £ 2)
Acidose respirat„ria aguda pH = 7,4 – [0,008 x (pCO2 – 40)]
Acidose respirat„ria cr•nica pH = 7,4 – [0,003 x (pCO2 – 40)]
Alcalose respirat„ria aguda pH = 7,4 + [0,008 x (40 – pCO2)]
Alcalose respirat„ria cr•nica pH = 7,4 + [0,017 x (40 – pCO2)]
OBS
5
: O conjunto cl•nico completo do paciente deve ser avaliado nos casos de dist‰rbios respirat„rios para
determinarmos se seu quadro ‚ agudo ou cr•nico. Para os exemplos a seguir, consideremos qualquer dist‰rbio
respirat„rio como agudo.
Caso 1.
pH arterial = 7,54
pCO2 = 23 mmHg
1.1. Existe dist‰rbio ƒcido-bƒsico, pois se observa um pH alto (7,54
- alcalose) e um pCO2 baixo (23mmHg).
1.2. Como o pH e o pCO2 est…o alterados, devemos observar a
dire†…o da mudan†a: se ambas se alteram em dire†ˆes
opostas, o dist‰rbio ‚ respirat„rio. Portanto, o dist‰rbio em
quest…o ‚ uma alcalose respiratória.
1.3. N…o ‚ necessƒrio realizar este passo, pois nem o pH nem o
pCO2 est…o normais.
2.2. Veremos se a varia†…o de pH estƒ adequada para uma alcalose
respirat„ria aguda (ver OBS5
):
pH = 7,4 + [0,008 x (40 – pCO2)]
pH = 7,4 + [0,008 x (40 – 23)]
pH = 7,54
Como o pH ‚ exatamente igual ao esperado, podemos concluir
que o paciente apresenta uma alcalose respirat„ria “pura” (ou
compensada).
R.: Alcalose respiratória pura.
Caso 2.
pH arterial = 7,32
pCO2 = 23 mmHg
HCO3 s‚rico =15 mEq/l
1.1. Existe dist‰rbio ƒcido-bƒsico, pois se observa um pH baixo
(7,32 - acidose) e um pCO2 baixo (23mmHg).
1.2. Como o pH e o pCO2 est…o alterados, devemos observar a
dire†…o da mudan†a: se ambas se alteram na mesma dire†…o,
que ‚ o caso, a desordem primƒria ‚ metab„lica. Portanto, o
dist‰rbio em quest…o ‚ uma acidose metabólica.
1.3. N…o ‚ necessƒrio realizar este passo, pois nem o pH nem o
pCO2 est…o normais.
2.1. Sendo o dist‰rbio uma alcalose metab„lica, devemos utilizar o
bicarbonato s‚rico nas equa†ˆes da tabela de compensa†…o
para se obter a pCO2 esperada. Desta forma, temos:
pCO2 = 1,5 x HCO3 + (8 £ 2)
pCO2 = 1,5 x 15 + (8 £ 2)
pCO2 = 22,5 + 8 £ 2
pCO2 esperada = 30,5 ± 2
O intervalo esperado ‚: 28,5 < pCO2 < 32,5. Contudo, a pCO2
em quest…o estƒ mais baixa (23mmHg) do que o esperado.
Tem-se, portanto, um dist‰rbio ƒcido-bƒsico secundƒrio,
causado por uma tentativa exagerada do organismo em
compensar o dist‰rbio primƒrio (o que significa que o organismo
estƒ eliminando mais CO2 do que o necessƒrio). Tem-se,
portanto, uma acidose metab„lica (dist‰rbio primƒrio) associada
a uma alcalose respirat„ria (dist‰rbio secundƒrio). Se, ao
contrƒrio, o pCO2 estivesse dentro desta faixa esperada,
ter•amos uma acidose metab„lica “pura” ou compensada.
2.2. N…o ‚ necessƒrio este passo.
R.: Acidose metabólica (distúrbio primário) associada a
uma alcalose respiratória (distúrbio secundário).](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-98-320.jpg)
![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
99
Caso 3.
pH = 7,22
pO2 = 70 mmHg
pCO2 = 70 mmHg
HCO3 = 23 mEq
1.1.Existe dist‰rbio ƒcido-bƒsico, pois se observa um pH
baixo (7,22 - acidose) e um pCO2 alto (70mmHg).
1.2.Como o pH e o pCO2 est…o alterados, devemos
observar a dire†…o da mudan†a: se ambas se alteram
em dire†ˆes opostas, o dist‰rbio ‚ respirat„rio.
Portanto, o dist‰rbio em quest…o ‚ uma acidose
respiratória.
1.3.N…o ‚ necessƒrio realizar este passo, pois nem o pH
nem o pCO2 est…o normais.
2.2. Veremos se a varia†…o do pH estƒ adequada para
este exuberante aumento de pCO2:
pH = 7,4 – [0,008 x (pCO2 – 40)]
pH = 7,4 - [0,008 x (70 – 40)]
pH = 7,16
Nota-se que o valor esperado para o pH era de 7,16,
isto ‚: esperava-se uma queda o pH bem maior,
quando comparado a este valor de pCO2. Portanto,
tem-se uma alcalose metab„lica secundƒria (pois o pH
medido ‚ maior do que o esperado). Se, ao contrƒrio,
o pH medido fosse de 7,16, tinha-se apenas uma
acidose respirat„ria “pura” (ou compensada).
R.: Acidose respiratória (distúrbio primário) associada
a uma alcalose metabólica (distúrbio secundário).
Caso 4.
pH 7,26
pCO2 = 68 mm Hg
pO2 = 53 mm Hg (90%)
HCO3 = 41 mEq
1.1.Existe dist‰rbio ƒcido-bƒsico, pois se observa um pH
baixo (7,26 - acidose) e um pCO2 alto (68mmHg).
1.2.Como o pH e o pCO2 est…o alterados, devemos
observar a dire†…o da mudan†a: se ambas se alteram
em dire†ˆes opostas, o dist‰rbio ‚ respirat„rio.
Portanto, o dist‰rbio em quest…o ‚ uma acidose
respiratória.
1.3.N…o ‚ necessƒrio realizar este passo, pois nem o pH
nem o pCO2 est…o normais.
2.2. Veremos se a varia†…o do pH estƒ adequada para
este exuberante aumento de pCO2:
pH = 7,4 – [0,008 x (pCO2 – 40)]
pH = 7,4 - [0,008 x (68 – 40)]
pH = 7,17
Nota-se que o valor esperado para o pH era de 7,17,
isto ‚: esperava-se uma queda o pH bem maior,
quando comparado a este valor de pCO2. Portanto,
tem-se uma alcalose metab„lica secundƒria (pois o pH
medido ‚ maior do que o esperado).
R.: Acidose respiratória (distúrbio primário) associada
a uma alcalose metabólica (distúrbio secundário).](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-99-320.jpg)
![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
100
Caso 5.
pH = 7,52
pCO2 = 20mmHg
HCO3 = 16mEq/l
pH alto; pCO2 baixo; HCO3 baixo Alcalose
respirat„ria.
pH = 7,4 + [0,008 x (40 – pCO2)]
pH = 7,4 + 0,16 pH esperado = 7,56
R.: Alcalose respiratória associada a uma acidose
metabólica.
Caso 6.
pH = 7,30
pCO2 = 27mmHg
HCO3 = 13mEq/l
pH baixo; pCO2 baixo; HCO3 baixo Acidose
metab„lica.
pCO2 = 1,5 x HCO3
-
+ (8 £ 2)
pCO2 = 19,5 + 8 (£ 2) pCO2 esperado = 27,5 ± 2
R.: Acidose metabólica pura (compensada).
Caso 7.
pH = 7,05
pCO2 = 55mmHg
HCO3 = 15mEq/l
pH baixo; pCO2 alto; HCO3 baixo Ac. respirat„ria.
pH = 7,4 - [0,008 x (pCO2 - 40)
pH = 7,4 – 0,12 pH esperado = 7,28
R.: Acidose mista (Ac. Respiratória + Ac. Metabólica)
Caso 8.
pH = 7,80
pCO2 = 48mmHg
HCO3 = 50mEq/l
pH alto; pCO2 alto; HCO3 alto Alc. metab„lica.
pCO2 = 0,7 + HCO3
-
+ (21 £ 2)
pCO2 = 35 + 21 (£ 2) pCO2 esperado = 56 ± 2
R.: Alcalose mista (Alc. Metabólica + Alc. Respiratória)
Caso 9.
pH = 7,42
pCO2 = 19mmHg
HCO3 = 12mEq/l
pH normal; pCO2 baixo; HCO3 baixo
Alc.respirat„ria.
pH = 7,4 + [0,008 x (40 - pCO2)
pH = 7,4 + 0,17 pH esperado = 7,57
R.: Alcalose respiratória associada a uma acidose
metabólica.
Caso 10.
pH = 7,42
pCO2 = 60mmHg
HCO3 = 38mEq/l
pH normal; pCO2 alto; HCO3 alto Ac. respirat„ria.
pH = 7,4 - [0,008 x (pCO2 - 40)
pH = 7,4 + 0,16 pH esperado = 7,24
R.: Acidose respiratória associada a uma alcalose
metabólica.](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-100-320.jpg)


![Arlindo Ugulino Netto – MEDICINA DE URG•NCIA – MEDICINA P8 – 2011.1
103
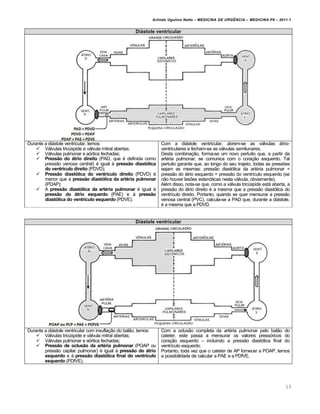
Disfun‚ƒo ventricular sistŠlica: se o ventrículo não é capaz de ejetar seu débito pré-determinado, o aumento
de pressão reflete no átrio e, posteriormente, na circulação pulmonar.
Cardiopatia isquêmica
Cardiopatia hipertensiva
Cardiopatia inflamatória
Valvopatias crônicas
Disfun‚ƒo ventricular diastŠlica: caracteriza-se pelo paciente que se apresenta com quadro clínico franco de
EAP, mas cuja radiografia de tórax mostra área cardíaca de dimensões preservadas.
Cardiopatia hipertrófica
Cardiopatia restritiva
Cardiopatia isquêmica
Cardiopatia hipertensiva
Sobrecarga vol•mica do ventr•culo esquerdo:
Insuficiência aórtica
Rotura do septo interventricular
Hipervolemia secundária a doença renal
Obstru‚ƒo da via de sa•da do ventr•culo esquerdo:
Estenose aórtica
Emergência hipertensiva
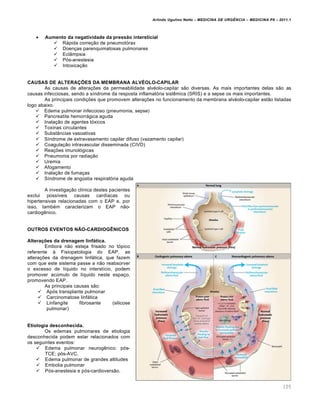
FISIOPATOLOGIA
Em duas condições fisiopatológicas ocorre a inundação dos alvéolos:
O desequilíbrio das forças que regem as trocas de fluido entre o meio intravascular e o interstício (Lei de Frank-
Starling)
Alterações da membrana alvéolo-capilar
DESEQUIL‰BRIO DAS FORŽAS DE STARLING
A Lei de Frank-Starling que rege as trocas de fluido entre o
meio intravascular e o interstício é representada pela seguinte
fórmula:
Q = K [(Phc – Phi) – (Pop – Poi)]
Q movimento do fluxo
K constante de permeabilidade
Phc Pressão hidrostática capilar
Phi Pressão hidrostática intersticial
Pop Pressão oncótica plasmática
Poi Pressão oncótica intersticial
Na prática, em nível capilar, sabe-se que existe um balanço entre forças e pressões que fazem com que sangue
saiam ou entrem no vaso. Desta forma, podemos destacar dois mecanismos:
Pressão hidrostática capilar e a pressão oncótica intersticial: favorecem a saída de líquido dos vasos para o meio
extracelular.
Pressão oncótica plasmática e a pressão hidrostática intersticial: favorecem a entrada de líquido dos vasos para
o meio intravascular.](https://image.slidesharecdn.com/medicinadeurgncia-completa-170904035246/85/Medicina-de-urgencia-completa-103-320.jpg)