1. A matéria é constituída de átomos, que são as menores partículas que identificam um elemento químico.
2. Os átomos são formados por um núcleo central com prótons e nêutrons, rodeado por elétrons. O número de prótons define o elemento químico.
3. As substâncias podem ser puras, formadas por um único tipo de átomo, ou misturas de vários tipos de átomos ou substâncias.

















![Módulo I – Unidade 1: Estrutura da Matéria
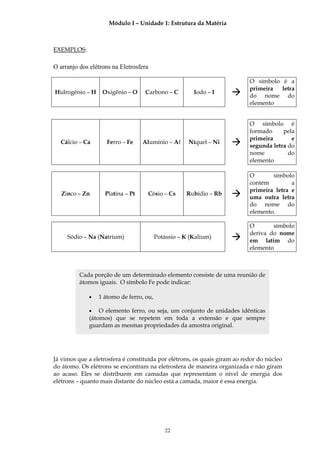
EXEMPLOS:
1) O hidrogênio 1H, que possui 1 elétron. Este permanece no subnível 1s, que entre
todos, possui menor energia. Dizemos que a distribuição eletrônica do 1H nos
subníveis é 1s1.
2) No caso do 2He, a distribuição é 1s2, ou seja, os seus 2 elétrons ocupam o subnível de
menor energia 1s.
3) O lítio 3Li apresenta distribuição 1s2 2s1, onde notamos que o terceiro elétron, não
cabendo no subnível 1s (que comporta no máximo 2), é forçado a ocupar o subnível 2s,
o qual, entre todos os demais, apresenta menor energia.
Observe agora, a configuração eletrônica de alguns átomos:
Átomo Configuração eletrônica
1H 1s1
2He 1s2 O símbolo [He] indica a
configuração eletrônica de
3Li 1s2 2s1 ou [He] 2s1
um átomo de hélio: 1s2.
4Be 1s2 2s2 [He] 2s2 Assim ao escrever que a
configuração de um átomo de
5B 1s2 2s2 2p1 [He] 2s2 2p1
3Li é [He]2s1, estamos
6C 1s2 2s2 2p2 [He] 2s2 2p2 querendo dizer que se trata
7N 1s2 2s2 2p3 [He] 2s2 2p3 de 1s2 2s1.Costuma-se chamar
o símbolo [He] de cerne de
8O 1s2 2s2 2p4 [He] 2s2 2p4 átomo de hélio. A
9F 1s2 2s2 2p5 [He] 2s2 2p5 configuração eletrônica
representada dessa maneira é
10Ne 1s2 2s2 2p6 [He] 2s2 2p6 chamada de configuração
11Na [Ne] 3s1 espectroscópica simplificada.
12Mg [Ne] 3s2
13Aℓ [Ne] 3s2 3p1
O símbolo [Ne] indica cerne
14Si [Ne] 3s2 3p2
de átomo de neônio, ou seja,
15P [Ne] 3s2 3p3 1s2 2s2 2p6.
16S [Ne] 3s2 3p4
17Cℓ [Ne] 3s2 3p5
18Ar [Ne] 3s2 3p6
19K [Ar] 4s1
O símbolo [Ar] indica cerne
20Ca [Ar] 4s2 de átomo de argônio, ou seja,
e assim por diante... 1s2 2s2 2p6 3s2 3p6.
31](https://image.slidesharecdn.com/mduloiunidade1contedo-100801171842-phpapp01/85/Mdulo-i-unidade-1-contedo-19-320.jpg)







![Módulo I – Unidade 1: Estrutura da Matéria
AGORA É COM VOCÊS:
6) As figuras representam as misturas de óleo com água e de álcool com água.
Assinale a alternativa correta.
a) Alcool e água em A, correspondendo o alcool a fase 2.
Recipiente A Recipiente B
b) Oleo e água em B.
fase 1 c) Alcool e água em A, correspondendo a água a fase 1.
fase 2 d) Oleo em água em A, correspondendo o oleo a fase1.
e) Oleo e água em A, correspondendo o oleo a fase 2.
7) (Funest – SP) Ar, iodo, gás carbônico, latão, naftalina, ouro 18 quilates. Se esses
materiais forem classificados em substâncias puras e misturas, pertencerão ao grupo
das substâncias puras:
a) ar, gás carbônico e latão.
b) iodo,ouro 18 quilates e naftaleno
c) gás carbônico, latão e iodo
d) ar, ouro 18 quilates e naftaleno
e) gás carbônico, iodo e naftaleno
8) Qual o número de massa e o número atômico de um átomo constituído de 17
prótons, 18 nêutrons e 17 elétrons?
Resolução: Z = p+ = 17; A = N0 + p+= 18 + 17 = 35.
9) Escreva as configurações eletrônicas para:
a) cada um dos átomos 17Cℓ, 12Mg, 10Ne.
Resolução: 10Ne : 1s2 2s2 2p6; 12Mg : 1s2 2s2 2p6 3s2 ou [Ne] 3s2; 17Cℓ : 1s2 2s2 2p6 3s2 3p5 ou [Ne] 3s2
3p5
b) cada um dos íons 17Cℓ-, 19K+, 13Aℓ3+
Resolução: 17Cℓ- : 1s2 2s2 2p6 3s2 3p6 ou [Ne] 3s2 3p6 ou [Ar]; 19K+ : 1s2 2s2 2p6 3s2 3p6 ou [Ne] 3s2 3p6
ou [Ar]; 13Aℓ3+ : 1s2 2s2 2p6 ou [Ne];
10) A corrosão de materiais de ferro envolve a transformação de átomos do metal em
íons (ferroso e férrico). Quantos elétrons há no terceiro nível energético do átomo
neutro de ferro?(Z=26). 3º nível mais energético = camada L→ 8 elétrons.
Resolução: 26Fe : 1s2 2s2 2p6 3s2 3p6 4s2 3d6
39](https://image.slidesharecdn.com/mduloiunidade1contedo-100801171842-phpapp01/85/Mdulo-i-unidade-1-contedo-27-320.jpg)