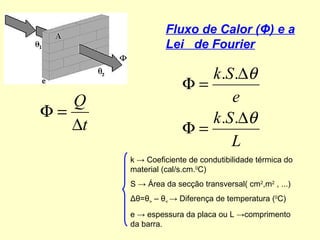
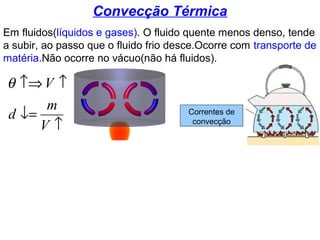
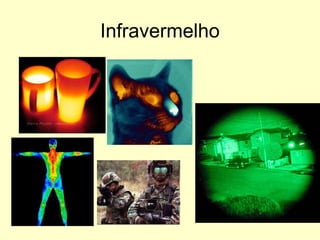
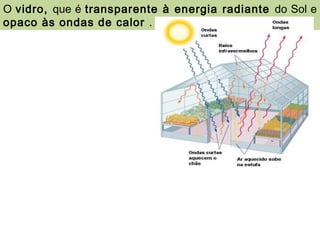
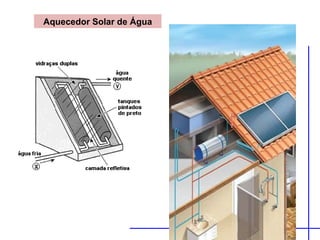
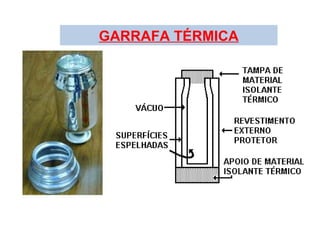
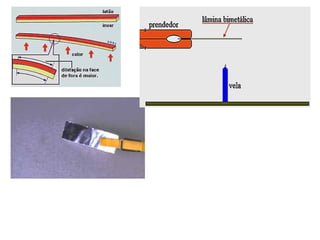
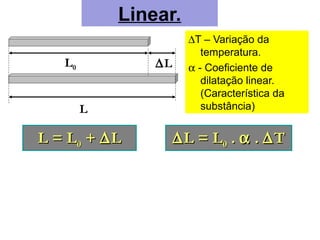
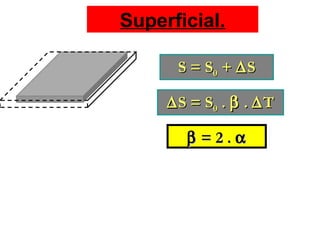
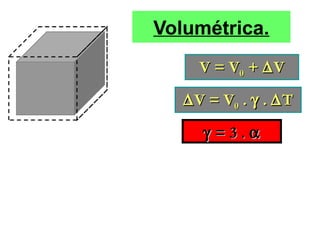
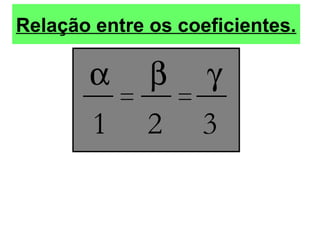
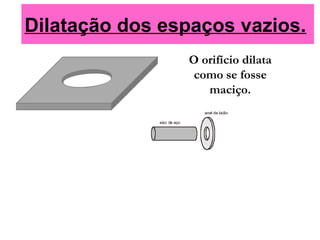
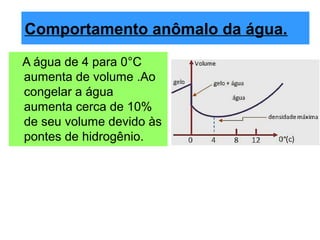
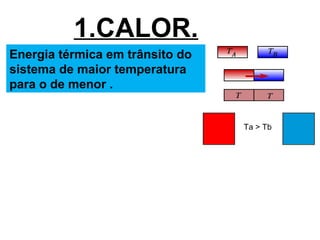
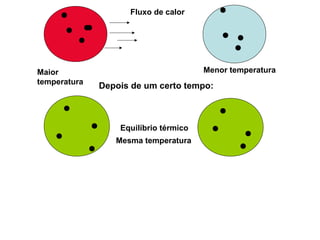
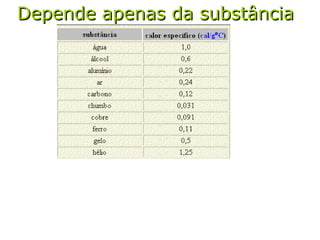
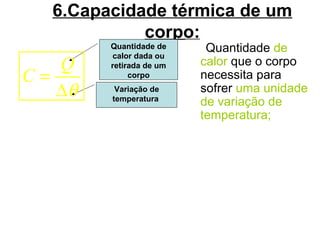
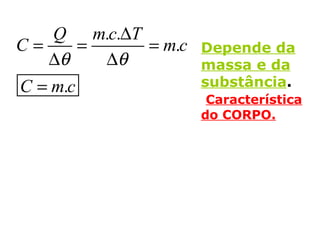
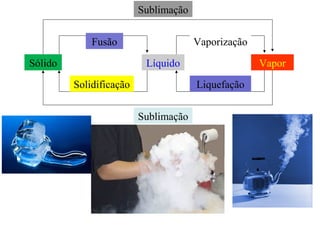
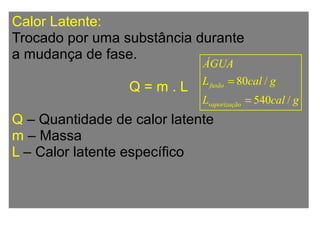
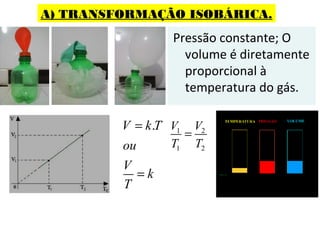
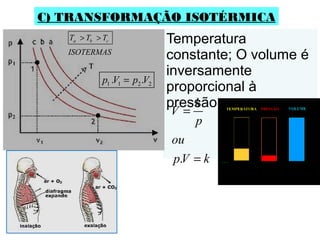
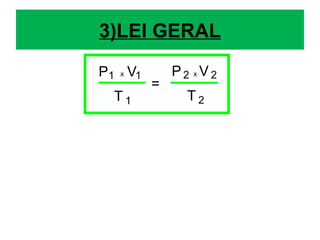
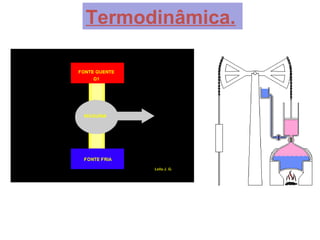
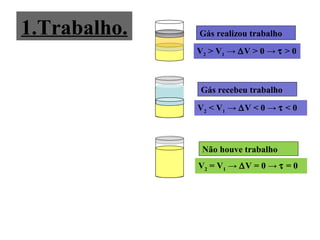
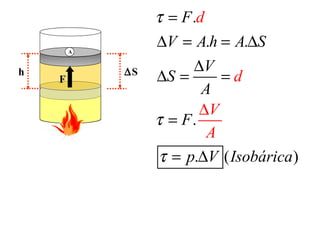
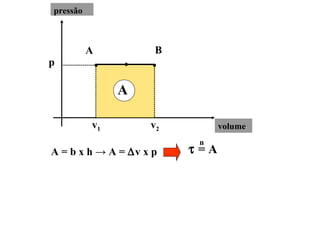
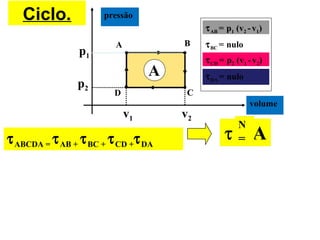
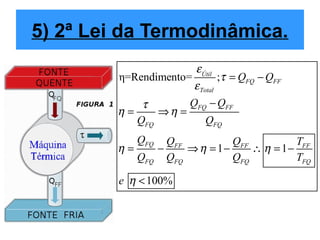
O documento discute os três mecanismos de transferência de calor: condução, convecção e radiação. A condução ocorre no contato direto entre moléculas, a convecção em fluidos como líquidos e gases, e a radiação propaga-se por ondas eletromagnéticas mesmo no vácuo. Além disso, aborda conceitos como coeficiente de condutibilidade térmica, dilatação térmica, mudança de fase, termodinâmica e máquinas térmicas.