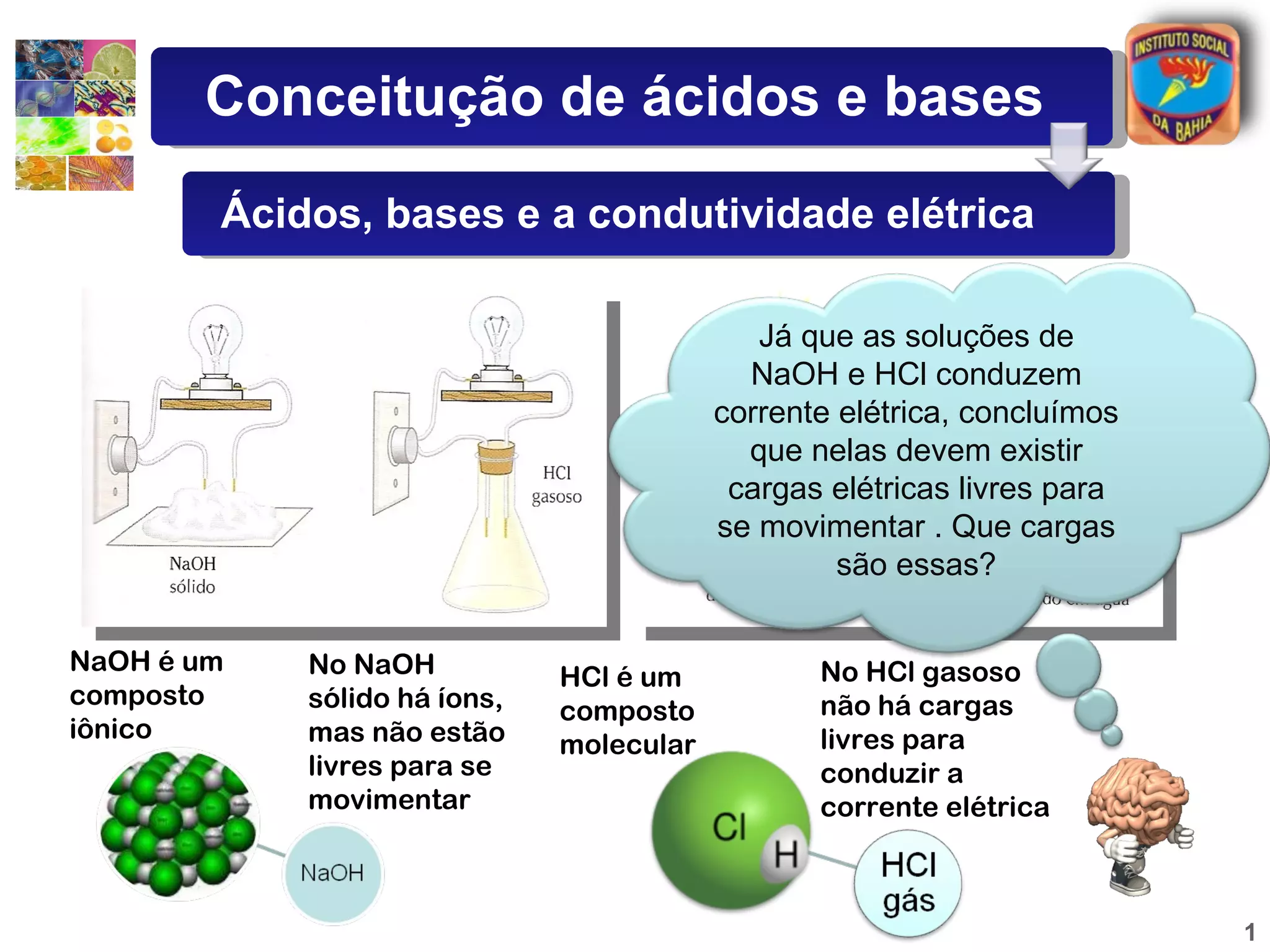
1) O documento discute conceitos de ácidos e bases segundo a teoria de Arrhenius.
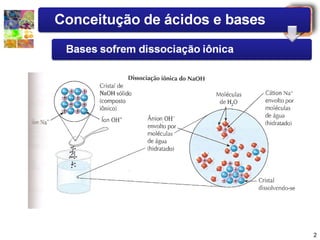
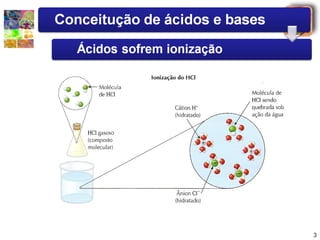
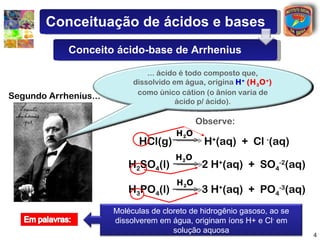
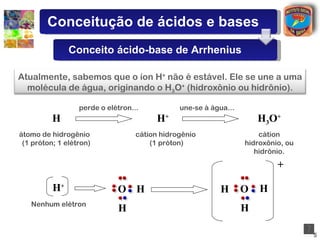
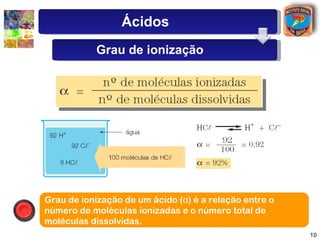
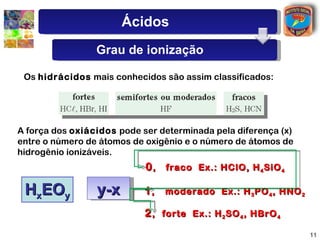
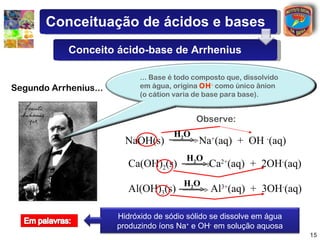
2) Arrhenius definiu ácidos como compostos que liberam íons hidrogênio quando dissolvidos em água e bases como compostos que liberam íons hidroxila.
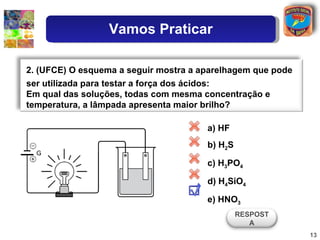
3) Exemplos de ácidos e bases são apresentados para ilustrar a teoria de Arrhenius.