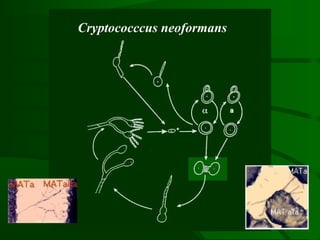
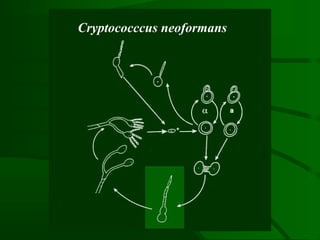
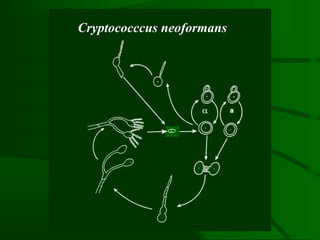
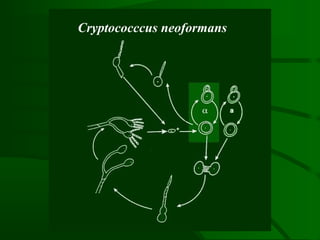
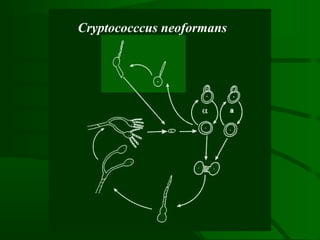
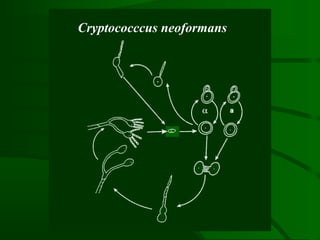
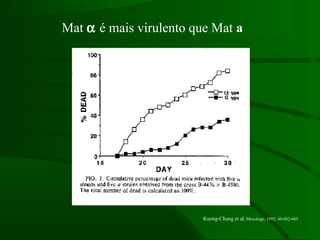
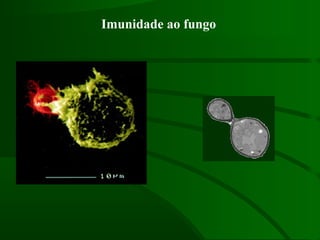
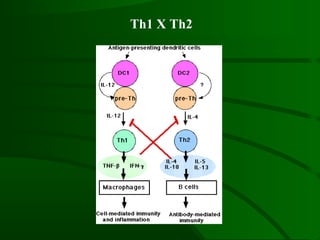
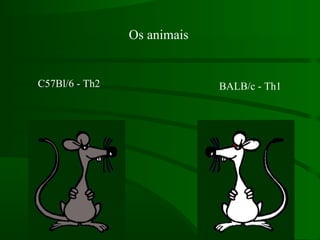
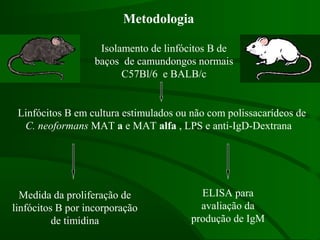
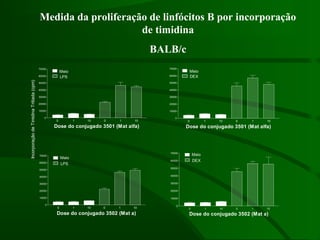
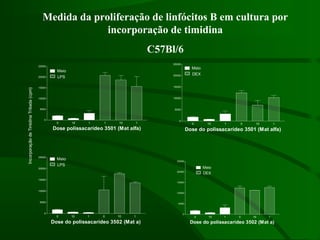
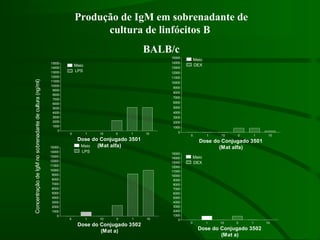
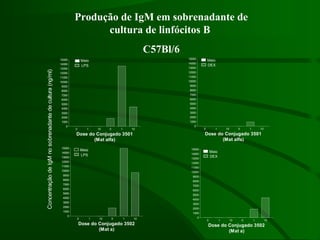
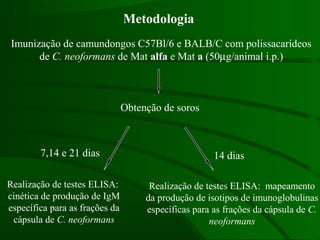
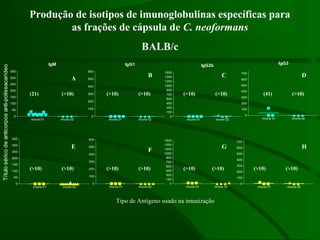
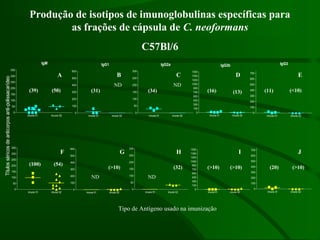
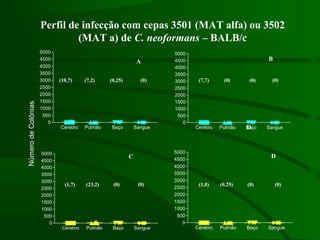
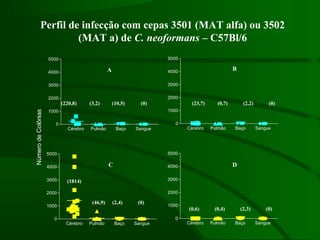
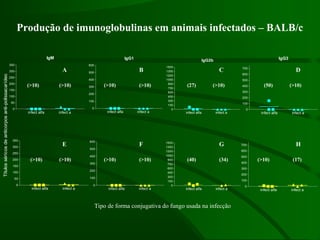
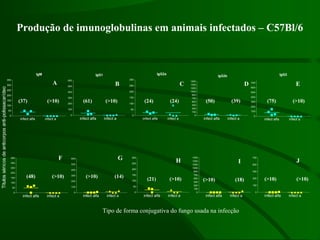
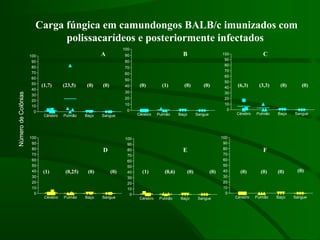
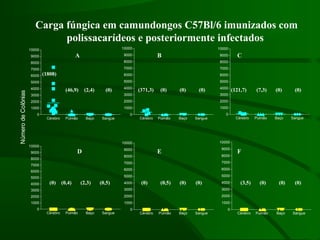
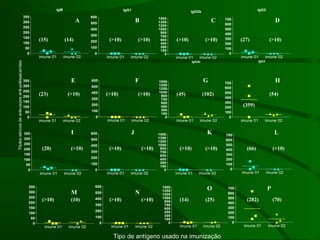
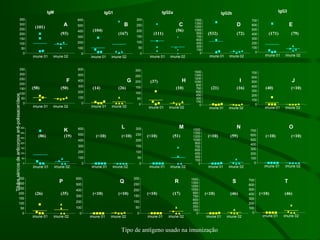
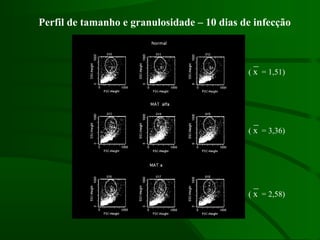
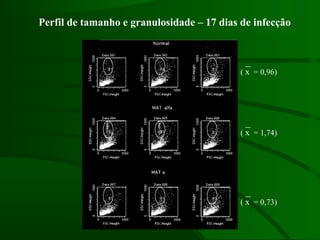
Este documento resume um estudo sobre a resposta de linfócitos B induzida por polissacarídeos de formas MAT alfa e MAT a de Cryptococcus neoformans em camundongos. Os principais achados são: (1) Os polissacarídeos induziram proliferação de linfócitos B e produção de IgM em cultura; (2) Camundongos imunizados produziram anticorpos específicos, principalmente IgG1 e IgG2b; (3) A resposta variou entre linhagens de camundongos e entre as form