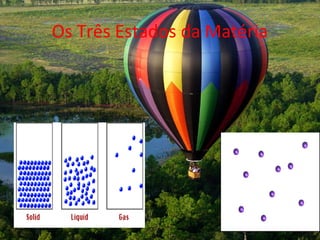
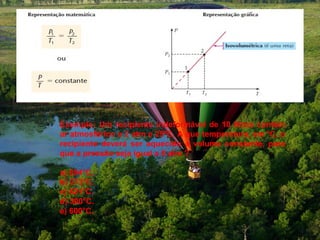
O documento apresenta as propriedades gerais dos gases, incluindo as leis de Boyle-Mariotte, Charles e Gay-Lussac. Discutem-se também pressão, unidades de pressão, volume molar e a equação de Clapeyron. Exemplos ilustram a aplicação destas leis e conceitos aos gases.