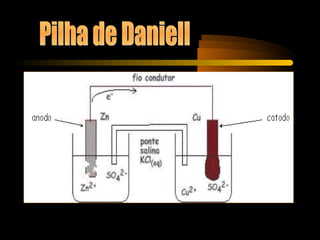
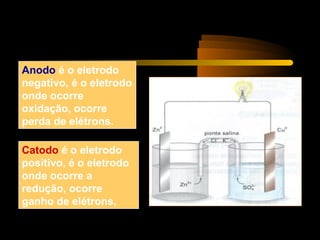
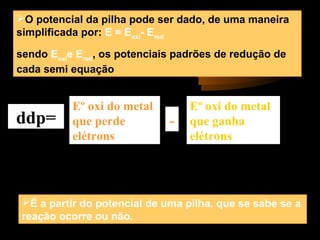
O documento discute o funcionamento de pilhas e baterias, desde as primeiras pilhas criadas por Volta e Daniell até baterias modernas. A pilha de Daniell foi uma melhoria da pilha de Volta, usando cátodos separados por uma ponte salina. O documento também explica conceitos como anodo, catodo e potencial eletroquímico.