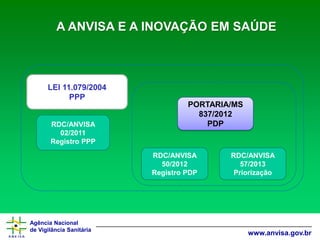
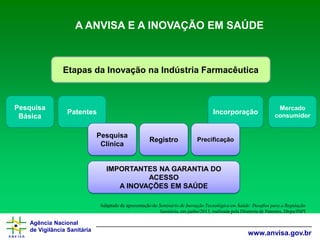
O documento discute como a ANVISA (Agência Nacional de Vigilância Sanitária) pode colaborar e participar ativamente da inovação em saúde no Brasil. Apresenta os marcos regulatórios da ANVISA relacionados à pesquisa clínica, registro e precificação de medicamentos inovadores. Também descreve os esforços da ANVISA para priorizar a análise de produtos inovadores e estimular a pesquisa clínica no país.











![Agência Nacional
de Vigilância Sanitária
www.anvisa.gov.br
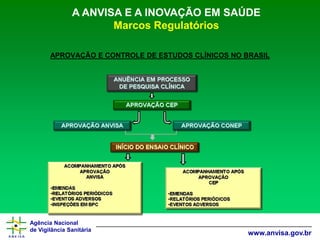
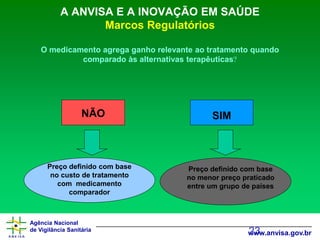
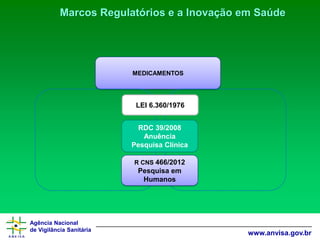
A ANVISA E A INOVAÇÃO EM SAÚDEMarcos Regulatórios
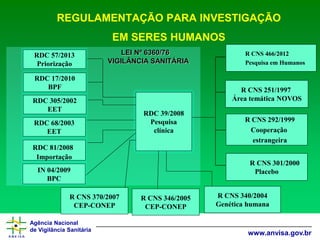
•LEINo6.360/76:DispõesobreaVigilânciaSanitáriaaqueficamsujeitososMedicamentos,asDrogas,osInsumosFarmacêuticoseCorrelatos, Cosméticos,SaneanteseOutrosProdutos,edáoutrasProvidências.
•Art.16.Oregistrodedrogas,medicamentos,insumosfarmacêuticosecorrelatos,[...],ficasujeito,[...],aosseguintesrequisitosespecíficos:
•II-queoproduto,atravésdecomprovaçãocientíficaedeanálise,sejareconhecidocomoseguroeeficazparaousoaquesepropõe,epossuaaidentidade,atividade,qualidade,purezaeinocuidadenecessárias;
•III-tratando-sedeprodutonovo,quesejamoferecidasamplasinformaçõessobreasuacomposiçãoeoseuuso,paraavaliaçãodesuanaturezaedeterminaçãodograudesegurançaeeficácianecessários;](https://image.slidesharecdn.com/08h20-dra-140829143530-phpapp02/85/37-Congresso-Brasileiro-de-Medicina-Farmaceutica-Dra-Marisa-Lisboa-14-320.jpg)