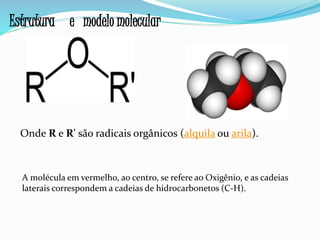
O documento discute os éteres, compostos orgânicos caracterizados por um átomo de oxigênio ligado a dois átomos de carbono. Detalha suas estruturas, propriedades, reações e métodos de síntese, incluindo a síntese de Williamson. Também apresenta exemplos como o éter etílico e aplicações dos éteres em medicina, indústria e como solventes.












![Reacções básicas
Os éteres têm comportamento de base de Lewis; reagem com
ácidos:
a) Com ácido sulfúrico (H2SO4)
H3C–O–CH3 + H2SO4(aq) → [H3C–O–CH3] HSO4
hidrogeno-sulfato de dimetil-oxônio
b) Com trifluoreto de boro (BF3)
H3C–O–CH3 + BF3 → [H3C–O–CH3]
eterato,fluoreto de Boro
H
̤
BF3
̤](https://image.slidesharecdn.com/estudodafamliadosteres-150603150636-lva1-app6892/85/Estudo-da-familia-dos-eteres-16-320.jpg)
![Formação de Peróxidos
Outra reacção dos éteres, que depende do par de electrões
livres no oxigénio é a que experimenta a temperatura
ambiente com o oxigénio atmosférico para formar Peróxidos:
H3C–O–CH3 + O2(g) → [H3C–O–CH3]
peróxido dimetílico
Esta reacção não tem nenhuma aplicação prática, mais representa
um grande perigo ao manusear éteres, porque os peróxidos são instáveis e
ao aquecer decompõem explosivamente
O2
̤](https://image.slidesharecdn.com/estudodafamliadosteres-150603150636-lva1-app6892/85/Estudo-da-familia-dos-eteres-17-320.jpg)



