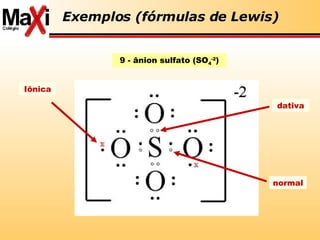
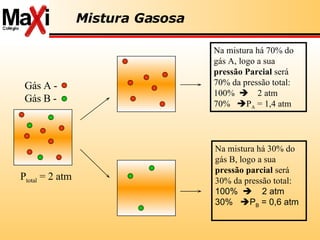
1) O documento discute vários conceitos químicos como leis de gases, unidades de concentração, métodos de separação de misturas e fórmulas de Lewis.
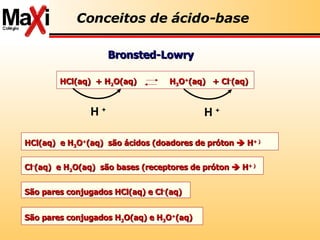
2) São apresentados os conceitos de ácido e base de acordo com as teorias de Arrhenius, Bronsted-Lowry e Lewis.
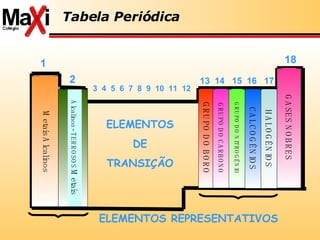
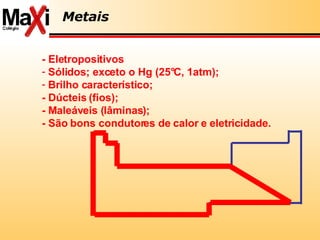
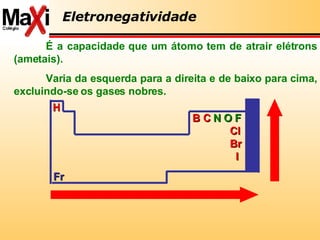
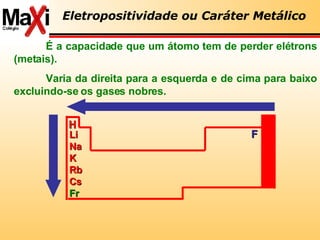
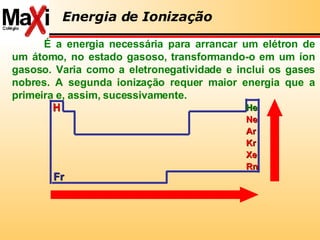
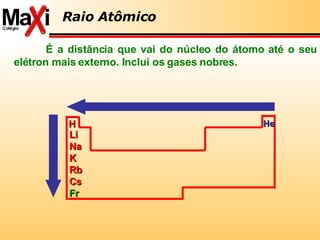
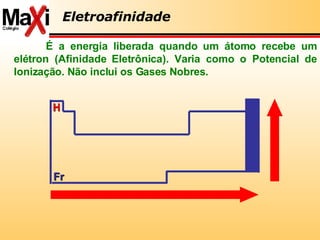
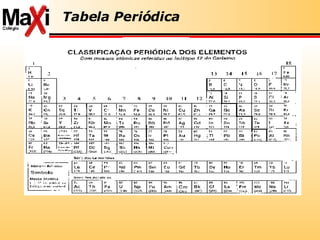
3) A tabela periódica é explicada com detalhes sobre propriedades dos elementos como eletropositividade, eletronegatividade e radioatividade.



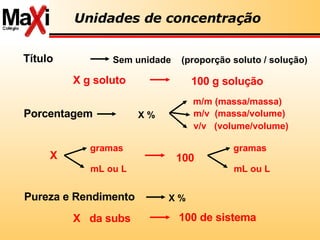

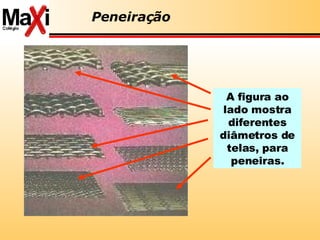




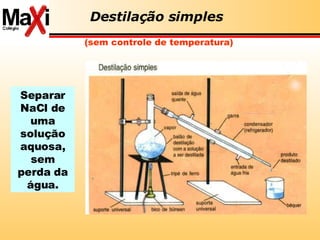
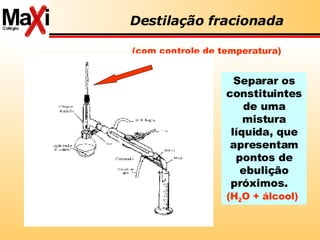







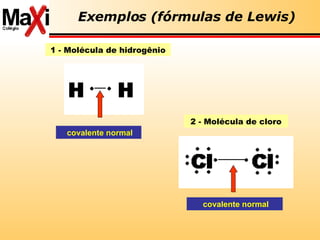
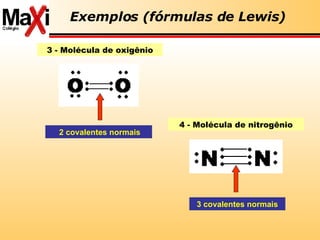
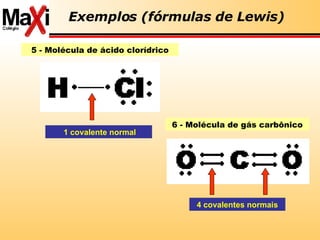
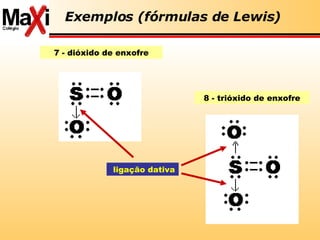






![ácido de Lewis: aceptor pares de elétrons base de Lewis: doador de pares de elétrons Lewis Conceitos de ácido-base Ácidos são substâncias receptoras de par eletrônico Cátios Bases são substâncias doadoras de par eletrônico Ânions H + (aq) + :OH - (aq) H 2 O Fe 3+ (aq) + SCN - (aq) [FeSCN] 2+( aq) H 3 N + BF 3 H 3 N:BF 3](https://image.slidesharecdn.com/reviso-para-ufmt-2008-1195302968222183-3/85/RevisaO-Para-Ufmt-2008-42-320.jpg)
